古老但仍然是最有用的制备联氨溶液的方法如下:NaClO+2NH3·H2O = N2H4 +NaCl+
| 古老但仍然是最有用的制备联氨溶液的方法如下:NaClO+2NH3·H2O = N2H4 +NaCl+3H2O (1)请在上述化学方程式中用单线桥法标出电子转移的方向和数目。 ___________________________________ (2)NH3·H2O在上述反应中显示出来的性质是_____________。 A.氧化性 B.还原性 C.酸性 D.碱性 (3)该反应的氧化产物是_____________,ClO-发生_____________反应。 (4)若生成 0.2mol N2H4,则转移的电子数为_____________mol 。 (5)请将上述反应改写为离子方程式__________________________ |
参考解答
(1)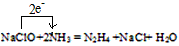 (2)B (3)N2H4;还原 (4)0.4 (5)ClO-+2NH3·H2O==N2H4+Cl-+3H2O |
相似问题
二氧化氮(NO2)是重要的空气污染物 科学家正寻求合适的 化合物G与适当的条件以进行如下反应 从而将
二氧化氮(NO2)是重要的空气污染物,科学家正寻求合适的 化合物G与适当的条件以进行如下反应,从而将二氧化氮转化为无毒的N2:NO2 + G→N2 +H2O +nY
“绿色试剂”双氧水可作为矿业废液消毒剂 如要消除采矿业废液中的氰化物(如KCN) 化学方程式为:K
“绿色试剂”双氧水可作为矿业废液消毒剂,如要消除采矿业废液中的氰化物(如KCN),化学方程式为:KCN+H2O2+H2O=A+NH3↑(1)生成物A的化学式为(2)
铁溶于一定浓度的硝酸溶液时 发生反应的离子方程式为:aFe+bNO3-+cH+=dFe2++fFe3
铁溶于一定浓度的硝酸溶液时,发生反应的离子方程式为:aFe+bNO3-+cH+=dFe2++fFe3++gNO↑+hNO2↑+kH2O.下列有关推断中,不正确的是( )A.2d+3f=3g+
一定物质的量SO2与NaOH溶液反应 所得产物中含Na2SO3和NaHSO3 则参加反应的SO2与N
一定物质的量SO2与NaOH溶液反应,所得产物中含Na2SO3和NaHSO3,则参加反应的SO2与NaOH的物质的量之比为可能为 [ ]A.1:1 B.1:2 C.3:5 D.2:1
亚硫酰氯(SOCl2)是重要的有机物卤化剂和电池的介质 生产上和生活中有着广泛应用 亚硫酰氯易水解
亚硫酰氯(SOCl2)是重要的有机物卤化剂和电池的介质,生产上和生活中有着广泛应用,亚硫酰氯易水解,在140℃以上可发生:4SOCl2=3Cl2↑+2SO2↑+S2Cl2。












