(4分)配平下列反应方程式并标出双线桥 KClO3+ KCl+ H2SO4 — Cl2↑
| (4分)配平下列反应方程式并标出双线桥 KClO3+ KCl+ H2SO4 — Cl2↑+ K2SO4+ H2O |
参考解答
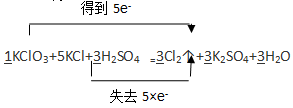 |
| 由反应前后的元素化合价变化可知KClO3作氧化剂(氯元素的化合价由+5价降低到0价),KCl作还原剂(氯元素的化合价-1价升高到0价),即氯气既是氧化产物又是还原产物,由电子的得失守衡可知氧化剂和还原剂的物质的量之比是1︰5。因此KClO3和KCl的计量数分别为1和5,然后通过观察法配平其它物质的计量数。 |
相似问题
高铁酸钾(K2FeO4)是一种新型 高效 多功能水处理剂。下列反应可制取K2FeO4:Fe2O3+3
高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂。下列反应可制取K2FeO4:Fe2O3+3KNO3+4KOH 2K2FeO4+3KNO2+2H2O。下列说法正确的是A.该反应是非氧
(6分)用双线桥法标出下列反应中电子转移的方向和数目 并回答下列相关问题:2KMnO4 + 16HC
(6分)用双线桥法标出下列反应中电子转移的方向和数目,并回答下列相关问题:2KMnO4 + 16HCl(浓) =" 2KCl" + 5Cl2↑ + 2MnCl2 + 8H2O(1)该反
在一定条件下 可发生反应:RO3n-+F2+2OH-==RO4-+2F-+H2O。则RO3n-中R元
在一定条件下,可发生反应:RO3n-+F2+2OH-==RO4-+2F-+H2O。则RO3n-中R元素的化合价是( )A.+4B.+5C.+6D.+7
(10分)实验室可用KMnO4和浓盐酸反应制取氯气。其变化可表述为:( )KMnO4+( )HCl(
(10分)实验室可用KMnO4和浓盐酸反应制取氯气。其变化可表述为:()KMnO4+( )HCl(浓) ===( )KCl+()MnCl2+()Cl2↑+()H2O(1)请配平化
将少量SO2通入Fe2(SO4)3溶液中发生反应:SO2+2Fe3++2H2O = SO42-+2F
将少量SO2通入Fe2(SO4)3溶液中发生反应:SO2+2Fe3++2H2O = SO42-+2Fe2++4H+;然后再加入K2Cr2O7溶液,发生反应:Cr2O72-+6Fe2++14H+ =2Cr3++6Fe3++7H2












