(7分)黄血盐[亚铁氰化钾 K4Fe(CN)6]目前广泛用做食盐添加剂(抗结剂) 我国卫生部规定食盐
(7分)黄血盐[亚铁氰化钾,K4Fe(CN)6]目前广泛用做食盐添加剂(抗结剂),我国卫生部规定食盐中黄血盐的最大使用量为10mg·kgˉ1。黄血盐易溶于水,在水溶液中会电离出K+和[Fe(CN)6]4ˉ,其中CNˉ的电子式为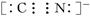 。它与硫酸反应的化学方程式为K4Fe(CN)6+6H2SO4+6H2O 。它与硫酸反应的化学方程式为K4Fe(CN)6+6H2SO4+6H2O 2K2SO4+FeSO4+3(NH4)2SO4+6CO↑ 2K2SO4+FeSO4+3(NH4)2SO4+6CO↑(1)上述反应是否为氧化还原反应?______ (填“是”或“不是”)。 (2)食盐经长时间火炒,“亚铁氰化钾”名称前的“亚铁”就去掉了,变成了剧毒物质氰化钾,这是因为黄血盐在超过4000C时会分解,试配平该反应的化学方程式: 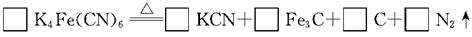 (3) 黄血盐可与高锰酸钾溶液反应,其化学方程式为 K4Fe(CN)6+ KMnO4+ H2SO4→KHSO4+ Fe2(SO4)3+MnSO4+HNO3+CO2↑+H2O(未配平) ①该反应的氧化产物有___ ___(填化学式)。 ②若有1mol K4Fe(CN)6被高锰酸钾氧化,则消耗高锰酸钾的物质的量为____ __mol。 |
参考解答
| (7分)⑴不是(1分) ⑵3,12,1,5,3(2分)⑶①Fe(SO4)3 、HNO3、CO2 (2分) ②12.2(2分) |
| (1)f反应中元素的化合价都没有发生变化,所以不是氧化还原反应。 (2)根据原子守恒可以进行配平。 (3)化合价升高的元素是铁元素、碳元素和氮元素,所以氧化产物是Fe(SO4)3 、HNO3、CO2。1mol K4Fe(CN)6在反应中失去电子是(1+2×6+8×6)mol=61mol,所以根据电子的得失守恒可知,消耗高锰酸钾的物质的量为61mol÷5=12.2mol. |
相似问题
对于反应3Cl2+6NaOH ==5NaCl+NaClO3+3H2O 以下叙述正确的是A.Cl2是氧
对于反应3Cl2+6NaOH ==5NaCl+NaClO3+3H2O,以下叙述正确的是A.Cl2是氧化剂,NaOH是还原剂B.被氧化的Cl原子和被还原的Cl原子的物质的量的比为5∶1C.Cl
向NaBr和KI混合溶液中通入足量氯气后 将溶液蒸干并灼烧 最后得到的物质是( )A.NaBr和KI
向NaBr和KI混合溶液中通入足量氯气后,将溶液蒸干并灼烧,最后得到的物质是()A.NaBr和KIB.NaBr和KClC.NaCl和KClD.NaCl、KCl和 I2
(4分)过氧化氢H2O2 (氧的化合价为-1价) 俗名双氧水 医疗上利用它有杀菌消毒作用来清洗伤口。
(4分)过氧化氢H2O2,(氧的化合价为-1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列A~D涉及H2O2的反应,填写空白:A.Na2O2 +2H
将3.48gFe3O4完全溶解于100mL0.5mol/L硫酸中 然后加入K2Cr2O7溶液25mL
将3 48gFe3O4完全溶解于100mL0 5mol L硫酸中,然后加入K2Cr2O7溶液25mL ,恰好使溶液中Fe2+全部转化为Fe3+,Cr2O72-全部还原为Cr3+,则K2Cr2O7溶液的物质
已知:异氰酸(HCNO)结构式为H—N=C=O 其中氮元素为-3价.HCNO能和NO2反应生成N2
已知:异氰酸(HCNO)结构式为H—N=C=O,其中氮元素为-3价.HCNO能和NO2反应生成N2、CO2、H2O 下列说法正确的是( )。A.在反应中,HCNO既被氧化又被












