碱金属与O2反应生成的氧化物比较复杂:有普通氧化物 如Na2O;过氧化物 如Na2O2;超氧化物 如
| 碱金属与O2反应生成的氧化物比较复杂:有普通氧化物,如Na2O;过氧化物,如Na2O2;超氧化物,如KO2;臭氧化物,如RbO3。其中后三种均可与水或CO2反应生成氧气。要制备普通氧化物,一般要用碱金属单质还原对应的过氧化物、硝酸盐或亚硝酸盐。 (1)用化学反应方程式表示①钠与Na2O2反应__________________________。②钾与硝酸钾反应:_____________________。③RbO3与CO2反应:______________________________。 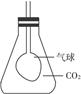 (2)若用锥形瓶收集一瓶CO2气体,在瓶内有一只扎紧在玻璃管末端的气球,如下图。打开塞子迅速往瓶里加入一种物质后,立即塞紧塞子,一段时间后气球就会自动膨胀,该物质可能是
|
参考解答
| (1)①2Na+Na2O2====2Na2O ②10K+2KNO3====6K2O+N2↑ ③4RbO3+2CO2====2Rb2CO3+5O2 (2)AB |
| (1)①钠具有还原性,Na2O2具有氧化性,二者可发生如下反应: 2Na+Na2O2====2Na2O ②同理根据题设,钾与硝酸钾反应时生成单质,则反应为10K+2KNO3====6K2O+N2↑。注意,此反应的最终产物为K2O而不是K2O2,因为K2O2能与K反应生成K2O。 ③类比过氧化钠与二氧化碳反应,可得4RbO3+2CO2====2Rb2CO3+5O2。 (2)气球会膨胀,表明瓶内气体压强减小(即气体总体积减小),答案为A、B。 |
相似问题
下列关于钠的说法不正确的是 (
下列关于钠的说法不正确的是()A.金属钠和氧气反应,条件不同,产物不同B.钠钾合金通常状况下呈液态,可作原子反应堆的导热剂C.钠的化学活泼性很强,
参照下表几种物质的溶解度 用固体NaOH 水 CaCO3(s) 盐酸为原料制取33 g纯NaHCO3
参照下表几种物质的溶解度,用固体NaOH、水、CaCO3(s)、盐酸为原料制取33 g纯NaHCO3晶体。25 ℃时溶解度 gNaHCO39Na2CO333NaOH110(1)若用水100 g,
2001年7月 有五只被人废弃的装金属钠的铁桶漂浮在珠江上 其中两只发生了剧烈爆炸 当时爆炸产生的白
2001年7月,有五只被人废弃的装金属钠的铁桶漂浮在珠江上,其中两只发生了剧烈爆炸,当时爆炸产生的白烟内还有许多没有燃烧的残渣,飘到附近后沉降下来,
两种钠盐晶体混合物 分装两支试管 其中一支加热时有CO2气体产生 另一支加水也有CO2气体产生。这两
两种钠盐晶体混合物,分装两支试管,其中一支加热时有CO2气体产生,另一支加水也有CO2气体产生。这两种盐可能是A.Na2CO3和NaHSO4B.NaHCO3和Na2HPO4C.N
对Na2O和Na2O2的叙述正确的是( )A.Na2O与Na2O2均可与HCl反应 故二者皆为碱性氧
对Na2O和Na2O2的叙述正确的是()A.Na2O与Na2O2均可与HCl反应,故二者皆为碱性氧化物B.Na2O与Na2O2在一定条件下可以相互转化C.Na2O和H2O反应为化合反












