(11分).A为单质 B C D E为与A含有相同元素的化合物 它们之间有如右图转化关系:(1)若右
(11分).A为单质,B、C、D、E为与A含有相同元素的化合物,它们之间有如右图转化关系: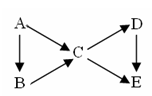 (1)若右图中B、C均为氧化物、D、E均为盐,则A可能是(填编号)__________。 ①Na ②N2 ③C ④S (2)若五种物质的焰色反应均为黄色,其中C、D、E的水溶液均显碱性,且等浓度时碱性C>D>E,B可做生氧剂,则B中含有的化学键类型为__________________; A转化成C的离子方程式为:________________________________, D转化成E的离子方程式为_______________________________________。 (3)若常温下B、C、D均为气体,且B气体能使湿润的红色石蕊试纸变蓝 ①在工业上生产B气体时为了加快反应速率应选择的条件是______________,其中能提高反应物的转化率的条件是___________。 ②C、D是汽车尾气中的有害成分,用NaOH溶液吸收可消除污染,反应的化学方程式为__________________________________。 |
参考解答
| (共11分)(1)①③(2分) (2)离子键、非极性共价键(或共价键);(2分)2Na+2H2O=2Na++2OH-+H2↑,(1分) CO32-+CO2+H2O=2HCO3? (1分) (3)①高温、高压、催化剂;(2分) 高压(1分) ②NO+NO2+2NaOH=2NaNO2+H2O(2分) |
(1)①③ 解析:①A→C:2Na+O2 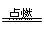 Na2O2,A→B:4Na+O2=2Na2O,B→C:2Na2O+O2 Na2O2,A→B:4Na+O2=2Na2O,B→C:2Na2O+O2 2Na2O2; 2Na2O2;②A→C,不能由N2直接生成NO2; ③A→C:C+O2  CO2,A→B:2C+O2='2CO' B→C:2CO+O2=2CO2; CO2,A→B:2C+O2='2CO' B→C:2CO+O2=2CO2;④A→C,不能由S直接生成SO3; (2)离子键、非极性共价键(或共价键);(2分)2Na+2H2O=2Na++2OH-+H2↑,(1分) CO32-+CO2+H2O=2HCO3? (1分) 解析:A、Na、B、为Na2O2、C为NaOH、D为Na2CO3、E 为NaHCO3,B、为Na2O2,Na+ 与O22―之间为离子键、O22―中O―O键为非极性共价键(或共价键);A转化成C的离子方程式为:)2Na+2H2O=2Na++2OH-+H2↑、D转化成E的离子方程式为CO32-+CO2+H2O=2HCO3? (3)①高温、高压、催化剂;(2分) 高压(1分) ②NO+NO2+2NaOH=2NaNO2+H2O(2分) 解析:A―N2 B―NH3 C―NO D―NO2 E―HNO3 ①在工业上生产NH3气体时为了加快反应速率应选择的条件是高温、高压、催化剂;其中能提高反应物的转化率的条件是高压;②C―NO、D―NO2是汽车尾气中的有害成分,用NaOH溶液吸收可消除污染,反应的化学方程式为NO+NO2+2NaOH=2NaNO2+H2O。 |
相似问题
(10分)将a mol的Na2O2和b mol NaHCO3固体混合后 在密闭容器中加热到250℃
(10分)将a mol的Na2O2和b mol NaHCO3固体混合后,在密闭容器中加热到250℃,让其充分反应,假设NaHCO3分解产生的CO2与Na2O2反应完后,H2O再与Na2O2
(8分)某同学欲探究与水的反应 可供使用的试剂有: 蒸馏水 酸性溶液 。该同学取一定量样品与过量水反
(8分)某同学欲探究与水的反应,可供使用的试剂有:、蒸馏水、酸性溶液、。该同学取一定量样品与过量水反应,待完全反应后,得到溶液X和一定量氧气,该
向某NaOH溶液中通入CO2气体后得溶液M 因CO2通入量的不同 溶液M的组成也不同。若向M中逐滴加
向某NaOH溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(盐酸)的关
将钠或过氧化钠投入到氯化亚铁溶液中 可观察到的共同现象是( )A.最终生成白色沉淀B.最终生成红
将钠或过氧化钠投入到氯化亚铁溶液中,可观察到的共同现象是()A.最终生成白色沉淀B.最终生成红褐色胶体C.有气泡产生D.无共同现象
下列实验方案中 可以测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是①取a克混合物与足
下列实验方案中,可以测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是①取a克混合物与足量稀盐酸充分反应,量取产生的气体体积为bmL(已折算为标况)②取a












