向盛有22.3g Na2CO3和NaCl固体混合物的烧杯中加入216.1g稀盐酸恰好反应 反应过程用
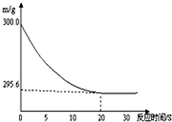
向盛有22.3g Na2CO3和NaCl固体混合物的烧杯中加入216.1g稀盐酸恰好反应,反应过程用精密仪器测得烧杯连同药品的质量(m)与反应时间(t)的关系如图所示:烧杯连同药品的起始质量为300g.下列分析计算结果错误的是( )
 |
参考解答
| A、反应曲线图可知,从20分钟时开始,曲线呈平直状态,说明反应已完全,故当固体混合物与稀盐酸恰好完全反应时,所需时间约为 20S; B、图示可知,完全反应后,纵坐标表示的药品质量为295.6,而未反应前是300,减少的部分正是反应过程中生成的二氧化碳气体的质量,故完全反应后,产生二氧化碳气体质量为300g-295.6g=4.4g; C、设参加反应的碳酸钠的质量为x,反应生成的氯化钠的质量为y Na2CO3+2HCl=2NaCl+H2O+CO2↑ 106 117 44 x y 4.4g
解之得:x=10.6g,y=11.7g; 故原固体中
D、反应后溶液总质量为:∴22.3g+216.1g-4.4g=234g;溶液溶质(NaCl)的质量为11.7g+(22.3g-10.6g)=23.4g 所得不饱和溶液的溶质质量分数:
故选C |
相似问题
将21g铁粉与足量的稀硫酸反应.计算:(1)生成的氢气和硫酸亚铁各多少克?(2)生成的氢气在标准状况
将21g铁粉与足量的稀硫酸反应.计算:(1)生成的氢气和硫酸亚铁各多少克?(2)生成的氢气在标准状况下的体积是多少升(氢气的密度是0 09g L,结果保留
一定质量溶质质量分数为19.6%的硫酸溶液与此同时13克锌恰好完全反应.试回答下列问题:(1)求硫酸
一定质量溶质质量分数为19 6%的硫酸溶液与此同时13克锌恰好完全反应.试回答下列问题:(1)求硫酸溶液的质量.(2)根据题条件,你还能求出______(写出
有两种金属混合物共30克 与足量稀硫酸反应 生成1克氢气 则这种混合物可能组成是( )A.Al 和
有两种金属混合物共30克,与足量稀硫酸反应,生成1克氢气,则这种混合物可能组成是( )A.Al和MgB.Fe和ZnC.Fe和MgD.Fe和Al
珍珠的某些成分具有药用价值 提取的过程是先将珍珠中大量的碳酸钙用浓盐酸除去(假设其他成分不与盐酸反应
珍珠的某些成分具有药用价值,提取的过程是先将珍珠中大量的碳酸钙用浓盐酸除去(假设其他成分不与盐酸反应且不含钙元素).经分析珍珠中碳酸钙的质量分
向硝酸银 硝酸铜 硝酸镁的混合溶液中加入一定质量的锌 充分反应后过滤 得到滤渣A和滤液B.(1)若反
向硝酸银、硝酸铜、硝酸镁的混合溶液中加入一定质量的锌,充分反应后过滤,得到滤渣A和滤液B.(1)若反应前后溶液质量不变,A中一定含有______.(2)若












