将50g铁片浸没在硫酸铜溶液中 片刻后取出 洗净 干燥 称得质量为52g 计算析出铜的质量。
| 将50g铁片浸没在硫酸铜溶液中,片刻后取出,洗净、干燥,称得质量为52g,计算析出铜的质量。 |
参考解答
反应后铁片质量增加了,原因是置换出来的铅覆盖在铁片上,且生成铜的质量大于反应掉的铁的质量。设析出铜的质量为x。 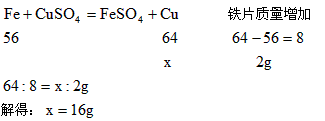 |
相似问题
已知碳酸氢钠(NaHCO3)受热易分解(2NaHCO3Na2CO3+CO2↑+H2O) 而碳酸钠受
已知碳酸氢钠(NaHCO3)受热易分解(2NaHCO3Na2CO3+CO2↑+H2O),而碳酸钠受热不分解。现取碳酸氢钠和碳酸钠的混合物Ag,加热到质量不再改变为止,剩余的
氢化锂(LiH)为玻璃状无色透明固体 军事上用作氢气发生来源 反应的化学方程式为:LiH+H2O==
氢化锂(LiH)为玻璃状无色透明固体,军事上用作氢气发生来源,反应的化学方程式为:LiH+H2O==LiOH+H2↑。计算80g氢化锂与足量的水反应生成氢气的质量。
物质R在0.96g氧气中恰好完全燃烧 反应方程式为:R+3O2XO2+2SO2 测得XO2和SO2的
物质R在0 96g氧气中恰好完全燃烧,反应方程式为:R+3O2XO2+2SO2,测得XO2和SO2的质量分别为0 44g和1 28g。下列判断正确的是[ ]A.参加反应的R的质量为0
胃舒平药片可用来治疗胃酸过多症 药片的标记如图所示 其主要成分是氢氧化铝[Al(OH)3] 请计算:
胃舒平药片可用来治疗胃酸过多症,药片的标记如图所示,其主要成分是氢氧化铝[Al(OH)3],请计算:(1)Al(OH)3中各元素的质量比:Al∶O∶H=________(
某化工厂生产的纯碱产品中含有少量氯化钠杂质 为测定该产品中含碳酸钠的质量分数 某课外兴趣小组进行了以
某化工厂生产的纯碱产品中含有少量氯化钠杂质,为测定该产品中含碳酸钠的质量分数,某课外兴趣小组进行了以下实验。取一定质量的该纯碱样品于试管中,加












