如右图所示 A为电源 B为浸透饱和食盐水和酚酞试 液的滤纸 滤纸中央滴有一滴KMnO4溶液 C
如右图所示,A为电源,B为浸透饱和食盐水和酚酞试 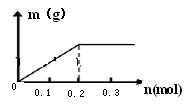 液的滤纸,滤纸中央滴有一滴KMnO4溶液,C、D为电解 槽,其电极材料及电解质溶液见图。 (1)关闭K1,打开K2,通电后,B的KMnO4紫红色液滴 向c端移动,则电源b端为 极,通电一段时间后, 观察到滤纸d端的电极反应式是: ; (2)已知C装置中溶液为Cu(NO3)2和X(NO3)3,且均为0.1mol,打开K1,关闭K2,通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如右图所示。 则Cu2+、X3+、H+氧化能力由大到小的顺序是 ; D装置中溶液是H2SO4,则电极Pt端的实验现象是: _____________________ 。 |
参考解答
| (1)-(负极)2H++2e=H2↑ (2)Cu2+ >H+ >X3+;在C端开始时有无色无味气体产生;一段时间后有红色物质析出。 |
| (1)据题意KMnO4紫红色液滴向c端移动,说明高锰酸根离子向c端移动,可推出c极为阳极,进一步可确定电源a端为正极,b端为负极。 (2)由右面图像可知,开始电解时,立即析出金属,说明开始H+没有放电,而是金属离子放电,据电极反应式:Cu2++2e-=Cu,可知0.1molCu2+全部析出,会得到0.2mol电子,若X3+得电子全部析出,会得到0.3mol电子,结合图像可确定开始Cu2+放电,Cu2+放电完后,没有金属析出,显然H+再放电,即氧化能力:Cu2+>H+ >X3+。电极Pt端为阴极,开始H+放电,阳极为铜电极,本身失电子,一段时间后,溶液中Cu2+的浓度增大,Cu2+会在阴极放电析出铜。 |
相似问题
如下图 x y分别是直流电源的两极 通电后发现a极板质量增加 b极板有无色无臭的气体放出 符合条件的
如下图,x、y分别是直流电源的两极,通电后发现a极板质量增加,b极板有无色无臭的气体放出,符合条件的是()a极板b极板x极板溶质A锌石墨负极CuSO4B石墨
将500mL0.1mol/L的CuSO4溶液和500mL4mol/L的NaCl溶液相混合 然后用石墨
将500mL0 1mol L的CuSO4溶液和500mL4mol L的NaCl溶液相混合,然后用石墨电极进行电解,电解过程中共有0 4mol电子通过。试计算:(1)阴极上可析出铜克。
下图为直流电源电解稀Na2SO4水溶液的装置 通电后在石墨电极a和b附近分别滴加石蕊溶液 下列实验现
下图为直流电源电解稀Na2SO4水溶液的装置,通电后在石墨电极a和b附近分别滴加石蕊溶液,下列实验现象正确的是[ ]A.逸出气体的体积:a电极的小于b电极的
利用如图装置 完成很多电化学实验.下列有关此装置的叙述中 正确的是( )A.若X为锌棒 Y为NaC
利用如图装置,完成很多电化学实验.下列有关此装置的叙述中,正确的是( )A.若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为
用石墨作电极电解CuCl2溶液 当通电一段时间后 收集到2.24L气体(标准状况).下列有关说法正确
用石墨作电极电解CuCl2溶液,当通电一段时间后,收集到2 24L气体(标准状况).下列有关说法正确的是( )A.阳极生成的铜B.上述电解过程中共转移0 2












