(12分)(1)有科学家提出“绿色自由”的构想:将CO2变为燃料或有机化学品。其构想分成3个步骤:①
| (12分)(1)有科学家提出“绿色自由”的构想:将CO2变为燃料或有机化学品。其构想分成3个步骤: ① 利用浓碳酸钾溶液吸收空气中的CO2; ② 将第①步吸收液电解产生H2和O2,同时分离出CO2; ③ 将第②步产生的H2和CO2在一定条件下转化成CH4和水蒸气。 已知:H2(g)+0.5O2(g)=H2O(l) △H1=" —285.8" kJ/mol CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H2=" —889.6" kJ/mol H2O(l)=H2O(g) △H3=" +44.0" kJ/mol 第③步反应的热化学方程式为 。 (2)使用合适的催化剂和电极材料,以N2、H2为原料,以HCl-NH4Cl为电解质溶液构成新型燃料电池,同时达到固氮作用。该电池的正极反应式为 ,溶液中H+向 极移动(选择填写“正”或“负”)。 (3)某催化剂的主要成分是FeO、Fe2O3,当催化剂中Fe2+与Fe3+的物质的量之比为1:2时,其催化活性最高。以Fe2O3为原料制备上述催化剂,可向其中加入适量炭粉,发生如下反应: 2Fe2O3+C 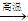 4FeO+CO2。为制得这种活性最高的催化剂,应向480 g Fe2O3粉末中加入炭粉的质量为_____g。 4FeO+CO2。为制得这种活性最高的催化剂,应向480 g Fe2O3粉末中加入炭粉的质量为_____g。(4)在T℃时,向2L固定体积的密闭容器中加入4 mol A和2 mol B,发生如下反应: 2A(g) + B(g)  C(g) + D(g) △H =" Q" kJ·mol-1 C(g) + D(g) △H =" Q" kJ·mol-1当反应达到平衡时,A的转化率为50﹪。 (ⅰ)在一定条件下,反应可以自发向右进行,可知Q __________0 (填“﹤”、“﹥”或“﹦”)。 (ⅱ)维持温度不变,若向该容器中加入的物质及量如下,使起始时v(正)>v(逆)且达到平衡时C的百分含量为20﹪。下列符合要求的是 A.2 mol A、1 mol B B.1 mol He、3 mol A、1.5 mol B、0.5molC、0.5mol D C.2 mol C、2 mol D D.2 molA、1mol B、1 mol C、1 mol D |
参考解答
| (1) CO2(g) + 4H2(g) = CH4(g) + 2H2O(g) △H = -165.6kJ/mol (2) N2+6e-+8H+=2NH4+ (3) 6 (4) < B |
| 略 |
相似问题
三氯化磷分子的空间构型是三角锥形而不是平面正三角形 下列关于三氯化磷分子空间构型理由的叙述 不正确的
三氯化磷分子的空间构型是三角锥形而不是平面正三角形,下列关于三氯化磷分子空间构型理由的叙述,不正确的是()A.PCl3分子中三个共价键的键长,键角都
下列反应属于吸热反应的是 ( )A.C6H12O6(葡萄糖aq)+6O26CO2+6H2OB.C
下列反应属于吸热反应的是 ()A.C6H12O6(葡萄糖aq)+6O26CO2+6H2OB.CH3COOH+KOH=CH3COOK+H2OC.A+B=C+D;ΔH <0D.反应物的键能大于生成物的键能
下列说法中正确的是( )A.全部由非金属元素形成的化合物一定是共价化合物B.溶于水可以导电的化合物
下列说法中正确的是()A.全部由非金属元素形成的化合物一定是共价化合物B.溶于水可以导电的化合物一定是离子化合物C.任何化学物质中均存在化学键D.
(8分)(1)实验室在配制氯化铁溶液时 常出现少许浑浊 原因离子方程式表示为
(8分)(1)实验室在配制氯化铁溶液时,常出现少许浑浊,原因离子方程式表示为 。为防止出现这样的现象,在配制时常加入(2)根据下列2个
下列物质中 既含有离子键又含有极性共价键的是A.Na2O2B.MgCl2C.HClD.NH4Cl
下列物质中,既含有离子键又含有极性共价键的是A.Na2O2B.MgCl2C.HClD.NH4Cl












