(6分)红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图
(6分)红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1 mol产物的数据)。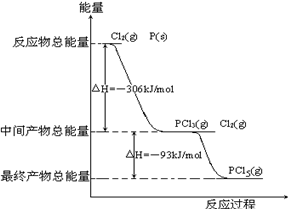 根据上图回答下列问题: (1)PCl3分解成P(s)和Cl2(g)的热化学方程式是__________________________________。 (2)P和Cl2分两步反应生成1 mol PCl5的△H1=_______________,与P和Cl2一步反应生成1 mol PCl5的△H2的关系是:△H2__________△H1(填“大于”、“小于”或“等于”)。 |
参考解答
| (1)2PCl3 (g) =' 3' Cl2 (g)+ 2P(s) ΔH=+612 kJ·mol-1 (2)-399 kJ·mol-1 等于 |
| (1)由图像可知P(s)和Cl2(g)的总能量高于PCl3(g),所以PCl3分解成P(s)和Cl2(g)的反应是吸热反应。因为每生成1mol PCl3(g),反应放出306kJ能量,故分解的热化学方程式为2PCl3 (g) =' 3' Cl2 (g)+ 2P(s) ΔH=+612 kJ·mol-1。 (2)根据图像可写出PCl3(g)和Cl2(g)反应生成1mol PCl5(g)的热化学方程式PCl3(g)+Cl2(g)反=PCl5(g) ΔH=-93 kJ·mol-1。所以根据盖斯定律知,将反应①2PCl3 (g) =' 3' Cl2 (g)+ 2P(s) ΔH=+612 kJ·mol-1和反应②PCl3(g)+Cl2(g)反=PCl5(g) ΔH=-93 kJ·mol-1叠加,即②-①÷2得到P(s)+5/2Cl2(g)反=PCl5(g),所以△H=-399 kJ·mol-1。反应热只与物质的始态和终态有关,而与反应过程无关,即△H2等于△H1。 |
相似问题
下表中的数据是破坏1 mol物质中的化学键所消耗的能量(kJ): 物质Cl2Br2I2H2键能
下表中的数据是破坏1 mol物质中的化学键所消耗的能量(kJ):物质Cl2Br2I2H2键能 kJ·mol-1243200151436下列物质本身具有的能量最低的是A.H2 B.Cl2 C.Br2 D.I2
(8分)有下列物质:①Cl2 ②Na2O2 ③NaOH ④HCl ⑤H2O2 ⑥MgF2 ⑦NH4C
(8分)有下列物质:①Cl2②Na2O2③NaOH④HCl⑤H2O2⑥MgF2⑦NH4Cl(1)属于离子化合物是___________;属于共价化合物是___________;(2)只由离子键构成的
据最新报道 科学家发现了如下反应:O2+PtF6 = O2PtF6 已知O2PtF6是离子化合物 其
据最新报道,科学家发现了如下反应:O2+PtF6 = O2PtF6,已知O2PtF6是离子化合物,其中阴离子为PtF6-。下列说法正确的是()A.该离子化合物中1mol阳
下列各组物质中 化学键类型不同的是( )A.NaCl和HNO3B.H2O和NH3C.CaF2和Cs
下列各组物质中,化学键类型不同的是( )A.NaCl和HNO3B.H2O和NH3C.CaF2和CsClD.CCl4和HCl
(18分)50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在下图所示的装置中进
(18分)50mL0 50mol L盐酸与50mL0 55mol LNaOH溶液在下图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:(1)












