(14分)50 mL 1.0 mol·L-1盐酸跟50 mL 1.1 mol·L-1氢氧化钠溶液在下
(14分)50 mL 1.0 mol·L-1盐酸跟50 mL 1.1 mol·L-1氢氧化钠溶液在下图装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热。试回答下列问题: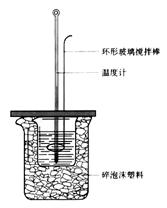 ⑴大小烧杯间填满碎泡沫塑料的作用___ 。 ⑵ (填“能”或“不能”)将环形玻璃搅拌棒改为环形铜棒。其原因是 。 ⑶大烧杯上如不盖硬纸板,对求得中和热数值的影响是 (填“偏高”或“偏低”或“无影响”)。 ⑷如果改用60 mL 1.0 mol·L-1盐酸跟50 mL 1.1 mol·L-1氢氧化钠溶液进行反应,则与上述实验相比,所放热量 (“增加”、 “减少”或“不变”),理由是 ;所求中和热数值 (“增加”、 “减少”或“不变”),理由是 。 |
参考解答
| ⑴减少实验过程中的热量损失 ⑵不能; 因金属易导热 ⑶偏低 ⑷增加;后者生成0.055mol的H2O,而前者只能生成0.050mol的H2O; 不变;“中和热”是指酸跟碱发生中和反应生成1摩尔H2O时所放出的热量,与酸碱的用量无关(每空2分) |
| (1)因为该实验中要尽可能的减少热量的损失,所以大小烧杯间填满碎泡沫塑料的作用减少实验过程中的热量损失。 (2)铜是热的良导体,易损失热量,所以不能将环形玻璃搅拌棒改为环形铜棒。 ⑶大烧杯上如不盖硬纸板,则热量会损失,测定结果偏低。 (4)改变酸、碱的用量,则反应中放出的热量发生变化,但中和热是不变的,因为中和热是指酸跟碱发生中和反应生成1摩尔H2O时所放出的热量,与酸碱的用量无关。 |
相似问题
下列化合物既含有共价键又含有离子键的是A.H2SO4B.Na2O2C.MgCl2D.C2H5OH
下列化合物既含有共价键又含有离子键的是A.H2SO4B.Na2O2C.MgCl2D.C2H5OH
关于氢键 下列说法正确的是:( )A.NH3在水中溶解度很大是由于NH3分子与NH3分子之间形成氢
关于氢键,下列说法正确的是:()A.NH3在水中溶解度很大是由于NH3分子与NH3分子之间形成氢键B.水是一种非常稳定的化合物,这是由于水分子之间能形成氢
下列说法不正确的是A.化学反应有新物质生成 并遵循质量守恒定律和能量守恒定律B.原子吸收光谱仪可用于
下列说法不正确的是A.化学反应有新物质生成,并遵循质量守恒定律和能量守恒定律B.原子吸收光谱仪可用于测定物质中的金属元素,红外光谱仪可用于测定化
实验测得 BeCl2为共价化合物 两个Be—Cl键间的夹角为180°则BeCl2属于A.由极性键构成
实验测得 BeCl2为共价化合物,两个Be—Cl键间的夹角为180°则BeCl2属于A.由极性键构成的极性分子B.由极性键构成的非极性分子C.由非极性键构成的极性
下列各组中的物质或离子都含配位键的是( )A.H2O Al2Cl6B.CO2 SO42-C.PCl
下列各组中的物质或离子都含配位键的是()A.H2O、Al2Cl6B.CO2、SO42-C.PCl5、[Co(NH3)4Cl2]ClD.NH4Cl、[Cu(NH3)4]SO4












