配位键是一种特殊的共价键 即共用电子对由某原子单方面提供和另一提供空轨道的粒子结合.如NH +4就是
配位键是一种特殊的共价键,即共用电子对由某原子单方面提供和另一提供空轨道的粒子结合.如NH
(1)下列粒子中可能存在配位键的是______. A.CO2 B.H3O+ C.CH4 D.NH
(2)硼酸(H3BO3)溶液呈酸性,试写出其电离方程式:______. (3)科学家对H2O2结构的认识经历了较为漫长的过程,最初科学家提出了两种观点: 甲: 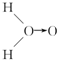 (式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂) 乙:HOOH化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验: a.将C2H5OH与浓H2SO4反应生成(C2H5)2SO4和水; b.将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4; c.将生成的A与H2反应(已知该反应中H2作还原剂). ①如果H2O2的结构如甲所示,实验c中化学反应方程式为(A写结构简式)______. ②为了进一步确定H2O2的结构,还需要在实验c后添加一步实验d,请设计d的实验方案:______. |
参考解答
| (1)H3O+中O提供孤电子对,H+提供空轨道,NH4+中N提供孤电子对,H+提供空轨道,二者都能形成配位键, 故答案为:BD; (2)硼原子为缺电子原子,H3BO3的电离是B原子和水电离的OH-形成配位键,水电离的H+表现酸性,反应的离子方程式为H3BO3+H2O=H++[B(OH)4-, 故答案为:H3BO3+H2O=H++[B(OH)4-; (3)①如果H2O2的结构如甲所示,实验c中A为 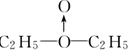 ,与氢气反应生成乙醚,方程式为 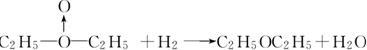 , 故答案为: 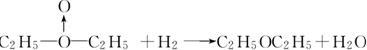 ; ②如为H0-OH结构,则A为C2H5-O-O-C2H5,与氢气反应生成乙醇,所以可用用无水硫酸铜检验c的反应产物中有没有水生成,如硫酸铜不变蓝,说明没有水生成,则说明过氧化氢中不含配位键,否则含有配位键, 故答案为:用无水硫酸铜检验c的反应产物中有没有水生成. |
相似问题
类推是化学学习和研究中常用的思维方法.下列类推错误的是①Mg可由电解熔融MgCl2制取;则Al也可由
类推是化学学习和研究中常用的思维方法.下列类推错误的是①Mg可由电解熔融MgCl2制取;则Al也可由电解熔融AlCl3制取②晶体中有阴离子,必有阳离子;则晶
下列判断正确的是 [ ]A.酸酐一定是氧化物 B.晶体中一定存在化学键 C.碱性氧化物一定是
下列判断正确的是 [ ]A.酸酐一定是氧化物 B.晶体中一定存在化学键 C.碱性氧化物一定是金属氧化物D.正四面体分子中键角一定是109°28′
试用杂化轨道理论说明下列分子或离子的几何构型。(1)CO2(直线形)_______________(
试用杂化轨道理论说明下列分子或离子的几何构型。(1)CO2(直线形)_______________(2)SiF4(正四面体形)________________(3)H2O(V形)________________ (4)NO2-(V形)________________
PtCl2(NH3)2可以形成两种固体 一种为淡黄色 在水中的溶解度小 另一种为黄绿色 在水中的溶解
PtCl2(NH3)2可以形成两种固体,一种为淡黄色,在水中的溶解度小,另一种为黄绿色,在水中的溶解度较大,请回答下列问题: (1)PtCl2(NH3)2是平面正方形结
下列分子的空间构型为V型的是( )A.H2OB.NH3C.HFD.CH4
下列分子的空间构型为V型的是( )A.H2OB.NH3C.HFD.CH4












