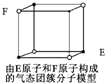
下列说法错误的是( )A.从CH4 NH4+ SO42-为正四面体结构 可推测PH4+ PO43-
下列说法错误的是( )
|
参考解答
| A.PH4+、PO43-中都形成4个б键,且孤电子对数分别为0,则应为正四面体结构,故A正确; B.金刚石晶体中,每个C原子与其它4个C原子形成共价键,且每2个C原子形成1个共价键,则1 mol金刚石晶体中,平均含有4mol×
C.氢键的作用力大于分子间作用力,H2O分子间存在氢键,H2S分子间不能形成氢键,导致水的沸点比硫化氢的高,故C正确; D.团簇分子中含有4个E、4个F原子,分子式应为E4F4或F4E4,故D错误. 故选D. |
相似问题
能说明CH4分子的5个原子不在同一平面而为正四面体构型的是 [ ]A.两个键之间
能说明CH4分子的5个原子不在同一平面而为正四面体构型的是[ ]A.两个键之间夹角为109°28′B.C-H键为极性共价键 C.4个C-H键的键能、键长相同D.碳的
下列不是配位化合物的是[ ]A.六氨合钴(Ⅲ)配阳离子[Co(NH3)6]3+ B.硝酸二氨
下列不是配位化合物的是[ ]A.六氨合钴(Ⅲ)配阳离子[Co(NH3)6]3+ B.硝酸二氨合银(I)[Ag(NH3)2]NO3 C.五水硫酸铜CuSO45H2O D.氯化铵NH4Cl
I 卤素化学丰富多彩 能形成卤化物 卤素互化物 多卤化物等多种类型的化合物.(1)①HClO4 ②H
I、卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物.(1)①HClO4、②HIO4、③H5IO6的酸性由强到弱的顺序为______(填序号)
乙炔是有机合成工业的一种原料 工业上曾用CaC2与水反应制备乙炔。(1)CaC2中C22-与O22+
乙炔是有机合成工业的一种原料,工业上曾用CaC2与水反应制备乙炔。(1)CaC2中C22-与O22+互为等电子体,O22+的电子式可表示为____________;1 mol O22+中
下列对分子结构叙述不正确的是[ ]A.H2O2分子中 两个O之间形成1对共用电子对B.N2的
下列对分子结构叙述不正确的是[ ]A.H2O2分子中,两个O之间形成1对共用电子对B.N2的电子式是N┇┇N C.CCl4和甲烷都是正四面体型分子D.CO2和CS2都是直线型分子