(三选一)【物质结构与性质】(1)金属钛(22Ti)将是继铜 铁 铝之后人类广泛使用的第四种金属 写
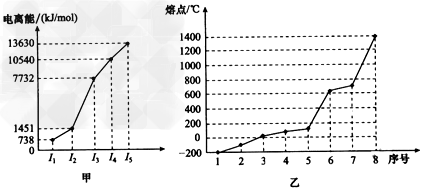
| (三选一)【物质结构与性质】 (1)金属钛(22Ti)将是继铜、铁、铝之后人类广泛使用的第四种金属,写出钛元素的基态原核外电子排布式:_______________ (2)日常生活中广泛应用的不锈钢,在其生产过程中添加了铬元素,该元素基态原子未成对电子数为_____________。 (3)COCl2俗称光气,分子中碳原子采取_____________杂化成键;其中碳氧原子之间的共价键含有____(填字母)。 a.2个σ键 b.2个π键 c.1个σ键、1个π键 (4)①短周期某主族元素M的逐级电离能情况如图甲所示,则M元素形成化合物时表现的主要化合价为______价。 ②第三周期8种元素按单质熔点高低的顺序如图乙所示,其中序号“8”代表_______(填元素符号,下同);其中电负性最大的是_________。 |
 |
| (5)由碳原子跟硅原子以1:1相互交替结合而形成的晶体,晶型与晶体Si相同。两者相比熔点更高的是________(填化学式),试从结构角度加以解释:______________ (6)在配合物Fe(SCN)2+中,提供空轨道接受孤对电子的微粒是_________________ |
参考解答
| (1)1s22s22p63s23p63d24s2 (2)6 (3)sp2;c (4)①+2;②Si;Cl (5)SiC;SiC晶体与晶体Si都是原子晶体,由于C的原子半径小,SiC中C-Si键的键长比晶体Si中Si-Si键的键长短,键能大,因而熔沸点更高 (6)Fe3+ |
相似问题
Q R X Y Z为前20号元素中的五种 Q的低价氧化物与X单质分子的电子总数相等 R与Q同族 Y和
Q、R、X、Y、Z为前20号元素中的五种,Q的低价氧化物与X单质分子的电子总数相等,R与Q同族,Y和Z的离子与Ar原子的电子结构相同且Y的原子序数小于Z。(1)Q
某同学在所收到的信封上发现有收藏价值的邮票 便将邮票剪下来浸入水中 以去掉邮票背面的黏合剂.根据“相
某同学在所收到的信封上发现有收藏价值的邮票,便将邮票剪下来浸入水中,以去掉邮票背面的黏合剂.根据“相似相溶”原理,该黏合剂的成分可能是( )A
下列有关甲醛分子的说法中正确的是[ ]A.C原子采取sp杂化 B.甲醛分子为三角锥形结构 C
下列有关甲醛分子的说法中正确的是[ ]A.C原子采取sp杂化 B.甲醛分子为三角锥形结构 C.C原子采取sp2杂化 D.甲醛分子为平面三角形结构
中学课堂实验提到 让蒸馏水通过酸式滴定管如线状慢慢流下 把摩擦带电的玻璃棒靠近水流 发现水流的方向发
中学课堂实验提到,让蒸馏水通过酸式滴定管如线状慢慢流下,把摩擦带电的玻璃棒靠近水流,发现水流的方向发生偏转。问:如果把盛在玻璃容器中的蒸馏水置
已知SO3 BF3 CCl4 PCl5 SF6都是非极性分子 而H2S NH3 NO2 SF4 Br
已知SO3、BF3、CCl4、PCl5、SF6都是非极性分子,而H2S、NH3、NO2、SF4、BrF5都是极性分子,由此可推出ABn型分子属于非极性分子的经验规律是( )A.AB












