(共8分)人类在使用金属的历史进程中 经历了铜 铁 铝之后 第四种将被广泛应用的金属被科学家预测为是
| (共8分)人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属被科学家预测为是钛(22Ti),它被誉为“未来世纪的金属”。 试回答下列问题: (1)Ti元素的基态原子的价电子层排布图为 ; (2)在Ti的化合物中,可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定; ①偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用。偏钛酸钡晶体中晶胞的结构示意图如图,它的化学式是 ;晶体内与每个“Ti”紧邻的氧原子数为 个。 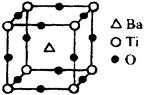 ②已知Ti3+可形成配位数为6的配合物。现有含钛的两种颜色的晶体,一种为紫色,另一种为绿色,但相关实验证明,两种晶体的组成皆为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验: a.分别取等质量的两种配合物晶体的样品配成待测溶液; b.分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀; c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的2/3。则绿色晶体配合物的化学式为 |
参考解答
| 1)电子排布图略 (2分)(2)①BaTiO3 (2分) 6 (2分) ②[TiCl(H2O)5Cl2·H2O(2分) |
(1)根据构造原理可知钛元素的价电子排布式是3d24s2,所以价电子排布图为
(2)根据晶胞的结构示意图可知钛位于顶点上,含有的个数是8×1/8=1,氧位于棱上,个数是12×1/4=3,钡位于体心,全部属于该晶胞,所以且化学式为BaTiO3。以顶点为中心向周围扩展,共有上下、左右和前后,所以有6个氧原子;根据沉淀质量可知绿色晶体配合物电离出的氯离子是紫色晶体电离出的2/3,这说明绿色晶体配合物中能电离的氯原子和不能电离的卤族是2︰1的,所以化学式为[TiCl(H2O)5Cl2 ·H2O。 |
相似问题
氮化硅(Si3N4)是一种新型的耐高温耐磨材料 在工业上有广泛用途 它属于A.原子晶体B.分子晶体C
氮化硅(Si3N4)是一种新型的耐高温耐磨材料,在工业上有广泛用途,它属于A.原子晶体B.分子晶体C.金属晶体D.离子晶体
据权威刊物报道 1996年科学家在宇宙中发现H3分子。甲 乙 丙 丁四位学生对此报道的认识正确的是
据权威刊物报道,1996年科学家在宇宙中发现H3分子。甲、乙、丙、丁四位学生对此报道的认识正确的是A.甲认为上述发现绝对不可能,因为H3分子违背了共价键
(9分)磷化硼(BP)和氮化硼(BN)是受到高度关注的耐磨涂料 它们的结构相似 右图为磷化硼晶体结构
(9分)磷化硼(BP)和氮化硼(BN)是受到高度关注的耐磨涂料,它们的结构相似,右图为磷化硼晶体结构中最小的重复结构单元。磷化硼可由三溴化硼和三溴化
如图是CsCl晶体的一个晶胞 相邻的两个Cs+的核间距为acm NA为阿伏加德罗常数 CsCl的相
如图是CsCl晶体的一个晶胞,相邻的两个Cs+的核间距为acm,NA为阿伏加德罗常数, CsCl的相对分子质量用M表示,则CsCl晶体的密度(g·cm-3)为( ) A.B.C.D.
下列说法正确的是( )A.冰融化时 分子中H—O键发生断裂B.分子晶体中 分子间作用力越大 通常熔
下列说法正确的是( )A.冰融化时,分子中H—O键发生断裂B.分子晶体中,分子间作用力越大,通常熔点越高C.分子晶体中,共价键键能越大,分子的熔、沸












