二氯化硫(S2Cl2)是一种琥珀色液体 是合成硫化染料的重要原料。它的熔点-80℃ 沸点138℃。常
| 二氯化硫(S2Cl2)是一种琥珀色液体,是合成硫化染料的重要原料。它的熔点-80℃,沸点138℃。常温下,它遇水易反应,产生使品红褪色的气体,且溶液出现浑浊。 (1)写出S2Cl2的电子式_____________________,该分子中Cl—S的键长_______S—S的键长(填“>”,“<”或“=”)。 (2)S2Cl2遇水反应产生气体,该气体分子的空间构型为 ,中心原子的杂化轨道类型为____ 。 (3)HF、H2S、HCl的稳定性由大到小的顺序为 ,沸点由高到低的顺序 为 。 (4)写出二氯化硫与水反应的化学方程式 。 |
参考解答
(1)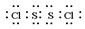 ; < ;(2)V形;sp2; ; < ;(2)V形;sp2;(3)HF>HCl>H2S ; HF>HCl>H2S ; (4)2S2Cl2+2H2O=SO2 ↑+3S↓+4HCl |
试题分析:(1)S2Cl2分子中S原子之间形成1对共用电子对,Cl原子与S原子之间形成1对共用电子对,电子式为 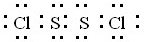 ;同周期自左向右原子半径逐渐减小,所以S原子半径大于氯原子半径,故Cl-S的键长<S-S的键长。 ;同周期自左向右原子半径逐渐减小,所以S原子半径大于氯原子半径,故Cl-S的键长<S-S的键长。(2)S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,。根据价层电子对互斥理论可知,S原子的孤对电子对数= 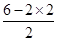 =1,价层电子对数=2+1=3,故二氧化硫为V形,S原子形成sp2杂化。 =1,价层电子对数=2+1=3,故二氧化硫为V形,S原子形成sp2杂化。(3)非金属性越强,氢化物的稳定性越强。非金属性F>Cl>S,因此氢化物稳定性是HF>HCl>H2S;氟化氢分子之间存在氢键,沸点最高,氯化氢与硫化氢都形成分子晶体,HCl的相对分子质量大,沸点比硫化氢高,故沸点由高到低的顺序为HF>HCl>H2S。 (4)S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,在反应过程中硫元素一部分升高到+4价(生成SO2),一部分降低到0价(生成S),由原子守恒可知还生成水,所以根据电子得失守恒可知反应方程式为2S2Cl2+2H2O=SO2↑+3S↓+4HCl。 |
相似问题
已知元素的某种性质“X”和原子半径 金属性 非金属性等一样 也是元素的一种基本性质。下面给出12种元
已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质。下面给出12种元素的X的数值:元素AlBBeCClFLiX的数值1 52 01 52
核内中子数为N的R2+ 质量数为A 则它的ng 氧化物中所含质子的物质的量是[ ]A.B.C
核内中子数为N的R2+,质量数为A,则它的ng 氧化物中所含质子的物质的量是[ ]A.B.C.D.
已知阴离子A2-的原子核内有x个中子 A原子的质量数为m 则Wg A2-含有电子的物质的量为 [
已知阴离子A2-的原子核内有x个中子,A原子的质量数为m,则Wg A2-含有电子的物质的量为 [ ]A.B. C.D.
下列对一些实验事实的理论解释正确的是
下列对一些实验事实的理论解释正确的是选项实验事实理论解释A.NH3溶于水形成的溶液微弱导电NH3是弱电解质B.氮气与氧气反应条件苛刻氮元素的非金属性不
三氟化硼(BF3)是一种无色气体 用于制造火箭的高能燃料。已知BF3是非极性分子 下列描述正确的是A
三氟化硼(BF3)是一种无色气体,用于制造火箭的高能燃料。已知BF3是非极性分子,下列描述正确的是A.BF3分子呈三角锥形B.BF3沸点低于BCl3C.B-F键键能












