核电荷数为1~18的元素的原子结构示意图等信息如下 回答下列问题:(1)在第二周期中 各原子结构的共
核电荷数为1~18的元素的原子结构示意图等信息如下,回答下列问题: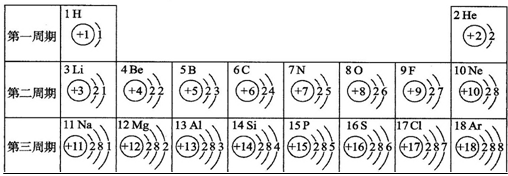 (1)在第二周期中,各原子结构的共同之处是 ;该周期中,各原子核外电子排布的变化规律是 。 (2)在第三周期中,元素类型的变化情况是:从左到右由 元素过渡到 元素,并以稀有气体元素结束。 (3)写出一个核外电子排布与氖原子相同的阳离子:阳离子 。 (4)一般地说,电子层数相同的原子(稀有气体除外),原子的半径随原子序数的递增而减小;最外层电子数相同的原子,原子的半径随电子层数的增加而增大。请比较:氮原子半径磷原子半径;氧原子半径 氟原子半径。(填“>”或“<”) |
参考解答
| (1)各原子的电子层数相同 最外层电子数依次递增 (2)金属 非金属 (3)Na+(Mg2+、Al3+) (4)< > |
试题分析:认真观察第二周期中,各原子的结构示意图不难发现,它们都有2个电子层,该周期中,各原子最外层电子数依次递增;在第三周期中,最左边的是金属元素然后过渡到非金属元素最后以稀有气体氩结束;氖的核外有2个电子层10个电子,失去电子后核外有10个电子的阳离子的原子主要有钠、镁和铝;由于氮和磷的最外层电子数相同且磷是3层,氮是2层,所以磷的原子半径比氮的原子半径大,由于氧和氟的电子层数相同,且氟的原子序数比氧的原子序数大,所以氧的原子半径大于氟的原子半径。 |
相似问题
与元素化学性质的关系最密切的是A.元素的相对原子质量B.原子核内的中子数C.原子核内的质子数D.原子
与元素化学性质的关系最密切的是A.元素的相对原子质量B.原子核内的中子数C.原子核内的质子数D.原子核外的最外层电子数
有下列物质:①洁净的空气;②液氮;③二氧化碳;④高锰酸钾加热后剩余的固体;⑤氯酸钾;⑥水银;⑦蒸馏水
有下列物质:①洁净的空气;②液氮;③二氧化碳;④高锰酸钾加热后剩余的固体;⑤氯酸钾;⑥水银;⑦蒸馏水。其中属于混合物的是(填序号),属于单质的
下图是钠与氯气反应生成氯化钠的模拟图。下列有关说法正确的是( )A.氯气 钠都由原子构成B.反
下图是钠与氯气反应生成氯化钠的模拟图。下列有关说法正确的是()A.氯气、钠都由原子构成B.反应中氯气分子分解成氯原子C.氯化钠由氯化钠离子构成D.
下列叙述正确的是A.纯碱 烧碱都属于碱B.棉花 羊毛都属于天然有机高分子材料C.化学反应中一定放出热
下列叙述正确的是A.纯碱、烧碱都属于碱B.棉花、羊毛都属于天然有机高分子材料C.化学反应中一定放出热量D.由两种元素组成的物质一定是化合物
树状分类法是日常生活和科学研究中常用的一种方法 如图所示的是一种树状分类的运用实例 下表所列的分类与
树状分类法是日常生活和科学研究中常用的一种方法,如图所示的是一种树状分类的运用实例,下表所列的分类与图分类不相符的是选项甲乙丙丁…A人体所需营养












