我国北方有许多盐湖 湖水中溶有大量的Na2CO3和NaCl 那里的人们冬天捞碱(Na2CO3) 夏天
| 我国北方有许多盐湖,湖水中溶有大量的Na2CO3和NaCl,那里的人们冬天捞碱(Na2CO3),夏天晒盐(NaCl).Na2CO3和NaCl的溶解度曲线如下图所示,据图回答下列问题: (1)t1℃时,溶解度较大的物质是______. (2)等质量Na2CO3、NaCl饱和溶液分别从t2℃降温到t1℃,析出晶体较多的是______. (3)冬天捞碱的原因是由于Na2CO3的溶解度随温度降低而______(填“增大”、“减小”或“不变”). (4)夏天晒盐是利用______(填序号)的方法,使NaCl晶体析出. ①升高温度,使NaCl溶解度增大 ②风吹日晒.使溶剂蒸发. 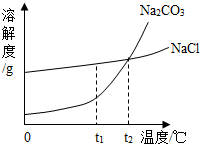 |
参考解答
| (1)由两物质的溶解度曲线不难看出,在t1℃时,氯化钠的溶解度大于碳酸钠的溶解度,故答案为:NaCl (2)由于氯化钠和碳酸钠的溶解度都随温度的升高而增大,但碳酸钠的溶解度受温度的影响较大,因此把等质量Na2CO3、NaCl饱和溶液分别从t2℃降温到t1℃,析出晶体较多的是碳酸钠,故答案为:碳酸钠 (3)冬天捞碱说明温度降低时,该物质的溶解度减小,故答案为:减小 (4)由于氯化钠的溶解度受温度的影响很小,因此若想使氯化钠从溶液中结晶析出,主要采取蒸发溶剂的方法,故答案为:② |
相似问题
已知下列现象和数据都是在20℃时所得.①取110g NH4Cl饱和溶液蒸发掉10g水后 析出晶体3.
已知下列现象和数据都是在20℃时所得.①取110gNH4Cl饱和溶液蒸发掉10g水后,析出晶体3 72g;②将120gNaNO3饱和溶液和50gNaNO3晶体共置于一个烧杯中,再
下列叙述正确的是( )A.温度升高时 物质的溶解度增大B.凡是均一 透明的液体就是溶液C.浓溶液不
下列叙述正确的是( )A.温度升高时,物质的溶解度增大B.凡是均一、透明的液体就是溶液C.浓溶液不一定是饱和溶液,稀溶液也不一定是不饱和溶液D.2
氯化钾和硝酸钾晶体在不同温度时的溶解度如下表所示:温度/溶解度/g物质010203040KCl27.
氯化钾和硝酸钾晶体在不同温度时的溶解度如下表所示:温度 溶解度 g物质010203040KCl27 631 034 037 040 0KNO313 320 931 645 863 9(1)30℃时KNO3的溶
如图是甲 乙两种固体物质的溶解度曲线.(1)从甲的饱和溶液中提取甲 适合用______方法.(2)t
如图是甲、乙两种固体物质的溶解度曲线.(1)从甲的饱和溶液中提取甲,适合用______方法.(2)t2℃时,将15g乙加入到盛有50g水的烧杯中,充分搅拌,所
将含有不溶性物质的硝酸钾固体的混合物放入一定量的水中充分搅拌 得到的实验数据如表1;硝酸钾在不同温度
将含有不溶性物质的硝酸钾固体的混合物放入一定量的水中充分搅拌,得到的实验数据如表1;硝酸钾在不同温度时的溶解度如表2:表1:温度 ℃204060剩余固体












