已知 :N2(g)+3H2(g) 2NH3(g) ΔH=-92 kJ·mol-1。(1) 在5
已知 :N2(g)+3H2(g)  2NH3(g) ΔH=-92 kJ·mol-1。 2NH3(g) ΔH=-92 kJ·mol-1。(1) 在500℃、2.02×107Pa和铁催化条件下2L密闭容器中充入1molN2和3mol H2,10 min时达到平衡,有0.2 mol NH3生成,则10 min内用氢气表示的该反应的平均速率v(H2)为 ,H2的转化率为__________。 (2)充分反应后,放出的热量______(填“<”“>”“=”)92.4kJ,理由是  。 。(3)为有效提高氢气的转化率,实际生产中宜采取的措施有____________
 |
参考解答
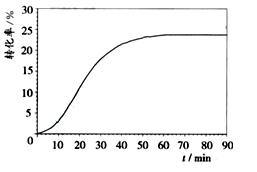
(1)0.01 5mol/(L·min)(2分),10%(2分) 5mol/(L·min)(2分),10%(2分)(2) <(1分); 在1atm和298K条件下,1mol氮气和3mol氢气完全反应生成2mol氨气,放出92.4kJ热量,该反应为可逆反应,反应物不能全部变为生成物;又因为反应温度为500℃,所以放出的热量小于92.4kJ(2分)。 (3)BEF(3分)。 (4) K= 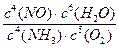 (2分); 减小(2分) (2分); 减小(2分) 作图要点:因为T2>T1,温度越高,平衡向逆反应方向移动,NH3的转化率下降,T2达到平衡时的平台要低于T1;另外温度越高,越快达到平衡,所以T2达到平衡的时间要小于T1。(2分) |
| 略 |
相似问题
COCl2(g) CO(g)+Cl2(g)- Q 当反应达到平衡时 分别采取下列措施 能使平衡向正反
COCl2(g) CO(g)+Cl2(g)- Q,当反应达到平衡时,分别采取下列措施,能使平衡向正反应方向移动的是A.恒容通入氮气B.恒压通入氮气C.加催化剂D.增加CO的浓度
在一定条件下 将物质的量相同的NO和O2混和 发生如下反应:2NO+O2=2NO2 2NO2N2O4
在一定条件下,将物质的量相同的NO和O2混和,发生如下反应:2NO+O2=2NO2,2NO2N2O4,所得混合气体中NO2的体积百分含量为40%,此时,混合气体的平均分子
在4L体积不变的密闭容器中充入6molA气体和5molB气体 发生反应:3A (g) + B (g)
在4L体积不变的密闭容器中充入6molA气体和5molB气体,发生反应:3A (g) + B (g)2C (g) + x D (g), 2分钟后反应达到平衡,生成了2molC,经测定
如图所示 容器A左侧是可平行移动的活塞。向A中充入1molX和1molY 向B中充入2molX和2m
如图所示,容器A左侧是可平行移动的活塞。向A中充入1molX和1molY,向B中充入2molX和2molY,起始时V(A)=V(B)=aL。在相同温度和有催化剂存在的条件下,两容
Ⅰ.已知溶液导电性与其中离子浓度有定量关系。某兴趣小组设计了以下装置和方法测定空气中SO2含量。你认
Ⅰ 已知溶液导电性与其中离子浓度有定量关系。某兴趣小组设计了以下装置和方法测定空气中SO2含量。你认为可行的操作是________________(填序号)Ⅱ Fe2+、












