有KCl和KBr的混合物3.87 g溶于水配成溶液 向溶液中加入足量的AgNO3溶液 得到6.63
有KCl和KBr的混合物3.87 g溶于水配成溶液,向溶液中加入足量的AgNO3溶液,得到6.63 g沉淀,则混合物中含K元素的质量分数约为( )
|
参考解答
| D |
| 初步审题,感觉是一道混合物的计算。仔细分析,可以发现KCl和KBr的混合物溶于水配成溶液,向溶液中加入足量的AgNO3溶液,得到沉淀,沉淀是AgCl和AgBr的混合物。3.87 g变成6.63 g,是K元素和Ag元素的质量差。 6.63 g - 3.87 g = 2.76 g K ~ Ag Δm 39 108 69 m(K) 2.76 g m(K)=39×2.76 g/108='1.56' g,混合物中含K元素的质量分数: 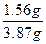 ×100%=40%。 ×100%=40%。 |
相似问题
氯水在空气中长期放置 不考虑水蒸发的情况下 下列微粒的物质的量会增多的是( )A.ClO-B.HC
氯水在空气中长期放置,不考虑水蒸发的情况下,下列微粒的物质的量会增多的是( )A.ClO-B.HClOC.水D.Cl-
如图是实验室中制备气体或验证气体性质的装置图.(1)仪器a的名称是______.(2)利用上图装置制
如图是实验室中制备气体或验证气体性质的装置图.(1)仪器a的名称是______.(2)利用上图装置制备纯净、干燥的氯气.①圆底烧瓶内发生反应的离子方程式
HClO是比碳酸还弱的酸 反应:Cl2+H2OHCl+HClO达平衡后 要使HClO浓度增加 可加入
HClO是比碳酸还弱的酸,反应:Cl2+H2OHCl+HClO达平衡后,要使HClO浓度增加,可加入A.H2S(气)B.HClC.CaCO3(固)D.H2O
能使干燥的红色布条褪色的是( )A.液氯B.新制氯水C.CaCl2溶液D.盐酸
能使干燥的红色布条褪色的是( )A.液氯B.新制氯水C.CaCl2溶液D.盐酸
A.它们都能以游离态存在于自然界B.它们的氧化物都能与强碱反应生成含氧酸盐C.气态氢化物的稳定性为C
A.它们都能以游离态存在于自然界B.它们的氧化物都能与强碱反应生成含氧酸盐C.气态氢化物的稳定性为CH4>SiH4D.N2和C在一定条件下分别与足量的O2反应,












