某学生设计如图所示实验装置利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应 反应后温度将升
| 某学生设计如图所示实验装置利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应,反应后温度将升高),A中盛浓盐酸,C中盛潮湿的消石灰,据此回答下列问题: (1)①烧瓶B中发生反应的化学方程式______. ②在该反应中所利用的浓盐酸的性质是:______.(填符号) a.酸性b.氧化性c.还原性d.碱性e.易挥发性 ③下列有关说法正确的是______.(以下气体体积都在标状况下测定) A.若提供0.4molHCl,MnO2不足量,则可制得氯气2.24L B.若提供0.4molHCl,MnO2过量,则可制得氯气2.24L C.若有0.4molHCl参加反应,可制得氯气2.24L D.若有0.4molHCl被氧化,可制得氯气2.24L (2)D中所盛的试剂是______,其作用是:______. (3)漂白粉将在U型管中产生,其化学反应方程式是______. (4)此实验结果所得Ca(ClO)2产率太低.经分析并查阅资料发现主要原因是在U型管C中存在两个副反应: ①温度较高时氯气与消石灰反应生成了Ca(ClO3)2,为避免此副反应的发生,可采取的措施是______. ②试判断另一个副反应是(写出此反应方程式)______.为避免此副反应发生,可采取的措施是______. 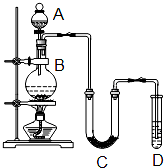 |
参考解答
(1)①加热条件下,二氧化锰和浓盐酸发生氧化还原反应生成氯气,反应方程式为:MnO2+4HCl(浓)
②该反应中,部分氯元素化合价升高,部分化合价不变,所以盐酸有还原性和酸性,故选ac; ③浓盐酸和二氧化锰反应生成氯气,但稀盐酸和二氧化锰不反应,且参加反应的盐酸有一半参加氧化还原反应,所以若有0.4molHCl参加反应,可制得氯气2.24L,故选C; 故答案为:MnO2+4HCl(浓)
(2)氯气有毒不能直接排空,但氯气能和氢氧化钠反应生成无毒物质,所以D中试剂是氢氧化钠溶液, 故答案为:NaOH溶液,吸收氯气等尾气,防止污染环境; (3)氯气和氢氧化钙反应生成氯化钙、次氯酸钙和水,反应方程式为:2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O,故答案为:2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O; (4)①温度较高时氯气与消石灰反应生成了Ca(ClO3)2,为避免副反应发生,应该降低温度,所以可以采取将U型管置于冷水浴中的措施, 故答案为:将U型管置于冷水浴中; ②盐酸易挥发,加热过程中生成的氯气中含有氯化氢,氯化氢能和碱反应,所以反应方程式为:Ca(OH)2+2HCl=CaCl2+2H2O,为避免副反应发生,可以在B、C之间连接一个盛有饱和食盐水的洗气瓶, 故答案为:Ca(OH)2+2HCl=CaCl2+2H2O;在B、C之间连接一个盛有饱和食盐水的洗气瓶. |
相似问题
氯气是一种有毒气体 在运输与储存过程中必须防止泄漏.一旦储存液氯的钢瓶发生泄漏 必须立即采取措施.下
氯气是一种有毒气体,在运输与储存过程中必须防止泄漏.一旦储存液氯的钢瓶发生泄漏,必须立即采取措施.下列各种措施不合理的是( )A.将人群向高处
标准状况下一充满氯气的试管插入水中 足够长时间后 试管内溶液液面稳定 则试管内溶液中溶质的物质的量浓
标准状况下一充满氯气的试管插入水中,足够长时间后,试管内溶液液面稳定,则试管内溶液中溶质的物质的量浓度为(假设溶质不向试管外扩散)( )A.0 0446
下列关于新制氯水和久置氯水的说法中 不正确的是( )A.新制氯水呈黄绿色 久置氯水无色B.新制的氯
下列关于新制氯水和久置氯水的说法中,不正确的是( )A.新制氯水呈黄绿色,久置氯水无色B.新制的氯水中无氯离子,久置的氯水中含有氯离子C.新制氯
自来水常用氯气进行消毒.用自来水配制下列溶液 不会产生明显药品变质的是( )A.FeCl2溶液B.
自来水常用氯气进行消毒.用自来水配制下列溶液,不会产生明显药品变质的是( )A.FeCl2溶液B.Na2SO3溶液C.NaOH溶液D. AlCl3溶液
新制氯水与久置的氯水相比较 下列结论不正确的是( )A.颜色相同B.前者能使有色布条褪色C.都含有
新制氯水与久置的氯水相比较,下列结论不正确的是( )A.颜色相同B.前者能使有色布条褪色C.都含有H+D.加AgNO3溶液都能生成白色沉淀












