(15分)某学习小组依据SO2具有还原性 推测SO2能被Cl2氧化生成SO2Cl2。查阅资料:SO2
| (15分) 某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2。 查阅资料:SO2Cl2常温下为无色液体,极易水解,遇潮湿空气会产生白雾。 Ⅰ.化合物SO2Cl2中S元素的化合价是 。 Ⅱ.用二氧化锰和浓盐酸制氯气的化学方程式是 。 Ⅲ.在收集氯气前,应依次通过盛有饱和食盐水和 的洗气瓶。 Ⅳ.用如图所示装置收集满Cl2,再通入SO2,集气瓶中立即产生无色液体, 充分反应后,将液体和剩余气体分离,进行如下研究。 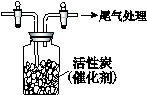 (1)研究反应的产物。向所得液体中加水,出现白雾,振荡、静置得到无色溶液。经检验该溶液中的阴离子(除OH-外)只有SO42-、Cl- ,证明无色液体是SO2Cl2。 ① 写出SO2Cl2与H2O反应的化学方程式 。 ② 检验该溶液中Cl-的方法是 。 (2)继续研究反应进行的程度。用NaOH溶液吸收分离出的气体,用稀盐酸酸化后,再滴加BaCl2溶液,产生白色沉淀。 ① 该白色沉淀的成分是 。 ② 写出SO2与Cl2反应的化学方程式,并阐述理由______。 |
参考解答
| (15分) I.+6价(2分); II.MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O(2分); MnCl2+Cl2↑+2H2O(2分);Ⅲ.浓硫酸(2分); Ⅳ.(1)① SO2Cl2+2H2O=H2SO4+2HCl (2分)。 ② 取少量该溶液于试管中,加入过量Ba(NO3)2溶液,过滤,向滤液中滴加 HNO3酸化,再加入AgNO3溶液,若产生白色沉淀,则说明溶液中有Cl-(2分); (2)① BaSO4(2分); ② SO2+Cl2  SO2Cl2 SO2Cl2由于白色沉淀是BaSO4,所以反应后的混合气体中必然存在SO2和Cl2两种气体。因此SO2和Cl2生成SO2Cl2的反应为可逆反应。(3分) |
试题分析:I.SO2能被Cl2氧化生成SO2Cl2则氯元素的化合价是-1价,O一般表现为-2价,所以S的化合价是+6价; II.实验室制取氯气的化学方程式为MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O; MnCl2+Cl2↑+2H2O;Ⅲ.SO2Cl2极易水解,遇潮湿空气会产生白雾,所以氯气必须是干燥的,因此在收集氯气前,应依次通过盛有饱和食盐水和浓硫酸的洗气瓶。 Ⅳ.(1)①根据元素的化合价,判断SO2Cl2水解的产物是硫酸和氯化氢,化学方程式为 :SO2Cl2+2H2O=H2SO4+2HCl ; ②检验该溶液中Cl-的方法是:因为溶液中有硫酸存在,所以检验氯离子前应除去硫酸根离子,取少量该溶液于试管中,加入过量Ba(NO3)2溶液,过滤,向滤液中滴加HNO3酸化,再加入AgNO3溶液,若产生白色沉淀,则说明溶液中有Cl-; (2)①若尾气中只含二氧化硫,被氢氧化钠吸收后滴加盐酸再滴加BaCl2溶液,不会产生白色沉淀。只含氯气也不会产生白色沉淀,所以尾气中有氯气和二氧化硫气体,白色沉淀是BaSO4 ②SO2+Cl2  SO2Cl2,由上面的分析可知反应后的混合气体中必然存在SO2和Cl2两种气体,若该反应不是可逆反应,则不可能2种反应物同时有剩余,所以SO2和Cl2生成SO2Cl2的反应为可逆反应。 SO2Cl2,由上面的分析可知反应后的混合气体中必然存在SO2和Cl2两种气体,若该反应不是可逆反应,则不可能2种反应物同时有剩余,所以SO2和Cl2生成SO2Cl2的反应为可逆反应。 |
相似问题
下列有关物质的性质和应用叙述正确并且有因果关系的是A.烧碱具有碱性 能用于治疗胃酸过多B.焦炭具有还
下列有关物质的性质和应用叙述正确并且有因果关系的是A.烧碱具有碱性,能用于治疗胃酸过多B.焦炭具有还原性,一定条件下能将二氧化硅还原为硅C.浓硝酸
从海水中提取的溴占世界溴年产量的1/3左右。已知溴水呈橙色 将SO2气体通入溴水时 可以使溴水褪色。
从海水中提取的溴占世界溴年产量的1 3左右。已知溴水呈橙色,将SO2气体通入溴水时,可以使溴水褪色。则下列有关叙述中正确的是( )。A.SO2使溴水褪色
下列实验中 不能观察到明显变化的是 [ ]A.把绿豆大的钾投入少量水中B.把一段打磨过的镁带
下列实验中,不能观察到明显变化的是 [ ]A.把绿豆大的钾投入少量水中B.把一段打磨过的镁带放入少量冷水中C.把溴水加入到淀粉KI溶液中D.氢气和氯气
用滴管将新制的饱和氯水慢慢滴入含酚酞的NaOH 稀溶液中 当滴到最后一滴时红色突然褪去。试回答下 列
用滴管将新制的饱和氯水慢慢滴入含酚酞的NaOH 稀溶液中,当滴到最后一滴时红色突然褪去。试回答下 列问题:(1)实验室保存饱和氯水的方法是____。(2)产
下列关于氯水的叙述 正确的是 [ ]A.新制氯水中只含Cl2和H2O分子B.新制氯水可使蓝色
下列关于氯水的叙述,正确的是 [ ]A.新制氯水中只含Cl2和H2O分子B.新制氯水可使蓝色石蕊试纸先变红后褪色 C.光照氯水有气泡逸出,该气体是Cl2 D.












