参考解答
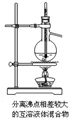
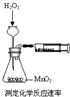
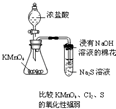
| A.温度计应位于蒸馏烧瓶的支管口附近,用于测量馏分的温度,故A错误; B.用长颈漏斗不能密封反应装置,导致气体逸散,应用分液漏斗,故B错误; C.碳酸酸性比苯酚强,碳酸氢钠与苯酚不反应,无法完成实验,故C错误; D.高锰酸钾与浓盐酸反应生成氯气,氯气可氧化硫化钠,溶液变浑浊,可通过反应现象判断氧化性强弱,故D正确. 故选D. |
相似问题
向NaBr NaI Na2SO3混合液中 通入一定量氯气后 将溶液蒸干并充分灼烧 得到固体剩余物质的
向NaBr、NaI、Na2SO3混合液中,通入一定量氯气后,将溶液蒸干并充分灼烧,得到固体剩余物质的组成不可能是( )A.NaCl,Na2S04B.NaCl,NaBr,Na2S04
三氟化氮(NF3)是无色无味气体 它可由氨气和氟气反应制得:4NH3+3F2=NF3+3NH4F。下
三氟化氮(NF3)是无色无味气体,它可由氨气和氟气反应制得:4NH3+3F2=NF3+3NH4F。下列说法正确的是 [ ]A NH4F的还原性比NH3强 B NF3的氧化性比F2强
已知:①2BrO3-+Cl2=Br2+2ClO3- ②5Cl2+I2+6H2O=2HIO3+10HC
已知:①2BrO3-+Cl2=Br2+2ClO3- ②5Cl2+I2+6H2O=2HIO3+10HCl ③ClO3-+5Cl-+6H+=3Cl2+3H2O 下列粒子氧化性强弱顺序正确的是[ ]A ClO3-
2010年诺贝尔化学奖授予美日科学家 他们由于研究“有机物合成过程中钯催化交叉偶联”而获奖。钯的化合
2010年诺贝尔化学奖授予美日科学家,他们由于研究“有机物合成过程中钯催化交叉偶联”而获奖。钯的化合物氯化钯可用来检测有毒气体CO,发生反应的化学方
已知在酸性条件下有如下关系:①KBrO3能把KI氧化成I2或KIO3 KBrO3本身被还原为Br2;
已知在酸性条件下有如下关系:①KBrO3能把KI氧化成I2或KIO3,KBrO3本身被还原为Br2;②Br2能把I-氧化成I2;③KIO3能把I-氧化成I2;④KIO3能把Br-氧化成Br