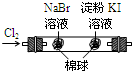
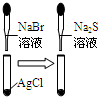
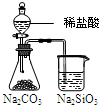
根据下列实验现象 所得结论正确的是( )实验实验现象结论A左烧杯中铁表面有气泡 右边烧杯中铜表面有
根据下列实验现象,所得结论正确的是( )
|
参考解答
| A、左边装置是电解池,较活泼的金属作电极时,在电流作用下阳极上是金属失电子,所以不能根据阴阳极上 得失电子判断金属的活泼性,原电池中较活泼的金属作负极,所以原电池中能根据正负极判断金属的活泼性,故A错误. B、氯气和溴化钠反应后有氯气剩余,氯气和溴都能和碘化钾置换出碘单质,氯气的存在影响溴的反应,所以右边棉花变为蓝色不能得出氧化性Cl2>Br2>I2,故B错误. C、左边溶液产生黄色沉淀,说明氯气的氧化性大于硫单质,右边溶液产生黄色沉淀说明溴的氧化性大于硫单质,但氯气和溴之间不发生反应,不能证明氯气和溴之间的氧化性强弱,故C错误. D、锥形瓶中有气体产生说明硫酸的酸性大于碳酸的酸性,烧杯中液体变浑浊说明碳酸的酸性大于硅酸的酸性,硫酸是硫元素的最高价含氧酸,所以能证明非金属性:S>C>Si,故D正确. 故选D. |
相似问题
Cl2的氧化性比S的氧化性强 最主要的事实是( )A.通常情况下硫为浅黄色固体 而氯气为黄绿色气体
Cl2的氧化性比S的氧化性强,最主要的事实是( )A.通常情况下硫为浅黄色固体,而氯气为黄绿色气体B.硫不溶于水,而氯气能溶于水C.与金属反应时,硫
在复杂体系中 确认化学反应先后顺序有利于解决化学问题.已知溶液中阳离子氧化性顺序为:Ag+>Fe3+
在复杂体系中,确认化学反应先后顺序有利于解决化学问题.已知溶液中阳离子氧化性顺序为:Ag+>Fe3+>Cu2+>H+>Fe2+>Na+,下列离子反应方程式错误的是
根据下列化学方程式:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O 2FeC
根据下列化学方程式:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O、2FeCl2+Cl2=2FeCl3、2FeCl3+2KI=2FeCl2+2KCl+I2,判断各物质氧化性由大到小的顺序正确的是
向含有Cu(NO3)2 Zn(NO3)2 Fe(NO3)3 AgNO3各0.1mol的混合溶液中加入
向含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3、AgNO3各0 1mol的混合溶液中加入0 1molFe,充分搅拌后Fe溶解,溶液中不存在Fe3+,同时析出0 1molAg..下列结
含有1mol FeBr2的溶液中 通入xmol Cl2.下列各项为通Cl2后 溶液内发生反应的离子方
含有1molFeBr2的溶液中,通入xmolCl2.下列各项为通Cl2后,溶液内发生反应的离子方程式,其中不正确的是( )A.x=1 5,2Fe2++4Br-+3Cl2→2Br2+2Fe3++