以下是原水处理成自来水的工艺流程示意图(1)原水中含Ca2+ Mg2+ HCO Cl-等 加入石灰后
 以下是原水处理成自来水的工艺流程示意图 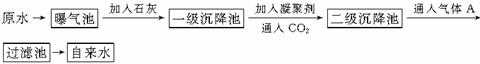 (1)原水中含Ca2+、Mg2+、HCO 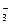 、Cl-等,加入石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式_________________________________ 、Cl-等,加入石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式_________________________________ (2)凝聚剂除去悬浮固体颗粒的过程 (填写编号,多选倒扣) ①只是物理过程 ②只是化学过程 ③是物理和化学过程FeSO4·7H2O是常用的凝聚剂,它在水中最终生成 沉淀。 (3)通入二氧化碳的目的是 和 。 (4)气体A的作用是 。这种作用是基于气体A和水反应的产物具有 性。 (5)下列物质中, 可以作为气体A的代用品。(填写编号) ①Ca(ClO)2 ②浓氨水 ③K2FeO4 ④SO2 |
参考解答
(1)HCO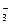 +OH-===CO +OH-===CO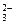 +H2O +H2OMg2++2OH-===Mg(OH)2↓ Ca2++HCO 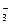 +OH-===CaCO3↓+H2O +OH-===CaCO3↓+H2O任选其一,其他合理解也给分。 (2)③ 胶状Fe(OH)3 (3)除去Ca2+ 调节pH (4)杀菌消毒 强氧化 (5)①③ |
(1)含Ca2+、Mg2+、HCO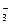 、Cl-的水中加入Ca(OH)2可发生多种反应:HCO 、Cl-的水中加入Ca(OH)2可发生多种反应:HCO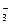 +OH-===CO +OH-===CO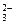 +H2O,Mg2++2OH-===Mg(OH)2↓,Ca2++HCO +H2O,Mg2++2OH-===Mg(OH)2↓,Ca2++HCO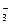 +OH-===CaCO3↓+H2O等等。 +OH-===CaCO3↓+H2O等等。(2)加入FeSO4·7H2O Fe2+被氧化为Fe3+,再水解生成胶状Fe(OH)3吸附水中杂质而沉淀。 (3)通入CO2目的,除去剩余Ca(OH)2,即Ca2+和OH-。 (4)气体A应为Cl2,因与水反应生成次氯酸具有强氧化性而杀菌消毒。 (5)应选强氧化剂。 |
相似问题
下列离子方程式中正确的是 A.碳酸钙和
下列离子方程式中正确的是A.碳酸钙和盐酸反应:CO32-+2H+=CO2↑+H2OB.过量的氯化铁和锌反应,锌溶解:2Fe3++Zn=2Fe2++Zn2+C.醋酸和苯酚钠溶液的反应:
(1)将NaAlO2(aq)和AlCl3(aq)混合: (水解相互促进
(1)将NaAlO2(aq)和AlCl3(aq)混合:(水解相互促进,反应进行到底,下同);(2)将10 00 mL 0 10 mol·L-1的NaHCO3(aq)与5 00 mL 0 10 mol·L-1的KAl(SO4)3(aq)混合:。
下列离子方程式正确的是
下列离子方程式正确的是()A.向滴有酚酞的硅酸钠溶液中滴加盐酸至浅红色: 2H++SiO2-4=H2SiO3(胶体)B.酸性条件下KIO3溶液与KI溶液发生反应生成I2:
下列物质间的反应属于离子反应的有哪些?能用离子方程式表示的写出离子方程式。⑴NaOH溶液与稀H2SO
下列物质间的反应属于离子反应的有哪些?能用离子方程式表示的写出离子方程式。⑴NaOH溶液与稀H2SO4反应。⑵固体食盐与浓H2SO4反应。⑶盐酸与石灰石反应
下列离子方程式正确的是
下列离子方程式正确的是()A.向次氯酸钙溶液中通入SO2:Ca2++2ClO-+SO2+H2O==CaSO3↓+2HClOB.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰使SO2-4沉淀完












