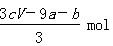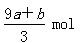a mol FeS与b mol Fe3O4投入到V L c mol·L-1的硝酸溶液中恰好完全反应
a mol FeS与b mol Fe3O4投入到V L c mol·L-1的硝酸溶液中恰好完全反应,假设只产生NO气体。所得澄清溶液的成分是Fe(NO3)3和H2SO4的混合液,则反应中未被还原的硝酸为
|
参考解答
| B |
| 设NO的物质的量为x,根据电子守恒得:3x=a+8a+b=9a+b, 所以混合溶液中,未被还原的HNO3的物质的量为 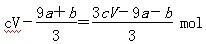 |
相似问题
a mol FeS与b mol FeO投入V L c mol·L-1的稀硝酸溶液中充分反应 产生NO
a mol FeS与b mol FeO投入V L、c mol·L-1的稀硝酸溶液中充分反应,产生NO气体,所得澄清溶液的成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中
工业上常利用反应 3Cl2 + 6KOH(热) → KClO3 + 5KCl + 3H2O 制取KC
工业上常利用反应 3Cl2 + 6KOH(热) → KClO3 + 5KCl + 3H2O 制取KClO3(混有KClO)。实验室模拟上述制备:在含溶质14mol的KOH(aq,热)中通入一
磷是地壳中含量较为丰富的非金属元素 主要以难溶于水的磷酸盐如Ca3(PO4)2等形式存在。它的单质和
磷是地壳中含量较为丰富的非金属元素,主要以难溶于水的磷酸盐如Ca3(PO4)2等形式存在。它的单质和化合物在工农业生产中有着重要的应用。(1)白磷(P4)可由C
下列说法正确的是( )A.常温常压下 22.4 L氯气与足量镁粉充分反应 转移的电子数为2NAB.
下列说法正确的是( )A.常温常压下,22 4 L氯气与足量镁粉充分反应,转移的电子数为2NAB.化合反应均为氧化还原反应C.电解NaCl溶液得到22 4 L H2(
(10分)将1.52g铜镁合金完全溶解于50.0mL密度为1.40g/mL 质量分数为63.0%的浓
(10分)将1 52g铜镁合金完全溶解于50 0mL密度为1 40g mL、质量分数为63 0%的浓硝酸中,得到NO2和N2O4的混合气体1120mL (标准状况),向反应后的溶液中加入