(8分)(1)向MnSO4和硫酸的混合溶液里加入K2S2O8(过二硫酸钾) 溶液会发如下反应:Mn2
| (8分)(1)向MnSO4和硫酸的混合溶液里加入K2S2O8(过二硫酸钾),溶液会发 如下反应:Mn2++S2O82-+H2O→MnO4-+SO42-+H+ 该反应常用于检验Mn2+的存在。其特征现象是_________________。 若反应中有0.1 mol还原剂参加反应,则消耗氧化剂物质的量__________mol。 (2)若该反应所用的硫酸锰改为氯化锰,当它跟过量的过硫酸钾反应时,除有高锰酸钾、硫酸钾、硫酸生成外,其他的生成物还有_________________。 (3)将NaBiO3固体(黄色微溶)加入到MnSO4和H2SO4的混合溶液里加热,固体溶解变为澄清溶液,发生如下反应: NaBiO3+ MnSO4+ H2SO4— Na2SO4+ Bi2(SO4)3+ NaMnO4+ H2O ①配平上述反应的化学方程式,并标出电子转移的方向和数目; ②上述反应中还原产物是 |
参考解答
| (1)溶液由无色变为紫色 0.25 (2)Cl2 (3)10 4 14 = 3 5 4 14 (2)Bi2(SO4)3 |
| (1)由于MnO4-在溶液中显紫红色,所以现象是溶液由无色变为紫色;还原剂是Mn2+,化合价从+2价升高到+7价,所以失去5个电子;氧化剂中S的化合价从+7价降低到+6价,得到1个电子,所以1mol氧化剂得到2mol电子,因此若反应中有0.1 mol还原剂参加反应,则消耗氧化剂物质的量0.25mol。 (2)由于在反应中氯离子也能被氧化,所以还生成氯气。 (3)根据方程式可知,Bi的化合价从+5价降低到+3价,得到2个电子。MnSO4中Mn的化合价从+2价升高到+7价,失去5个电子,所以氧化剂是NaBiO3,还原剂是MnSO4,二者的物质的量之比是5︰2,其中还原产物是Bi2(SO4)3,氧化产物是NaMnO4,因此方程式为 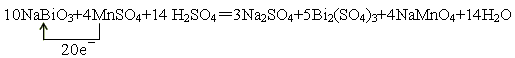 |
相似问题
下列各组物质由于浓度不同而能发生不同氧化还原反应的是( )①Cu与HNO3溶液;②NaOH与Al
下列各组物质由于浓度不同而能发生不同氧化还原反应的是()①Cu与HNO3溶液;②NaOH与AlCl3溶液;③Zn与H2SO4溶液;④Na与O2反应A.①③B.①②③C.②③④D.①④
(8分)某反应中反应物与生成物有:KClO3 K2SO4 H2C2O4 CO2 H2SO4 H2O和
(8分)某反应中反应物与生成物有:KClO3、K2SO4、H2C2O4、CO2、H2SO4、H2O和一种氧化物X。(1)已知KClO3在反应中得到电子,则该反应的还原剂是。(2)
根据反应8NH3 + 3Cl2 ='=' 6NH4Cl+ N2 回答下列问题:(1) 还原剂是
根据反应8NH3 + 3Cl2 ="=" 6NH4Cl+ N2 ,回答下列问题:(1) 还原剂是(写化学式);(2) 用双线桥法表示该反应电子转移的方向和数目;(3)当反应
(6分)实验室可以用高锰酸钾和浓盐酸反应制取氯气 反应如下:KMnO4 + HCl(浓) → KCl
(6分)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应如下:KMnO4 + HCl(浓) → KCl + MnCl2 + Cl2↑ + H2O(1)配平反应方程式:KMnO4 +H
某铁的氧化物 用7mol/L的盐酸100mL在一定条件下恰好完全溶解 所得溶液再通入0.56L氯气时
某铁的氧化物,用7mol L的盐酸100mL在一定条件下恰好完全溶解,所得溶液再通入0 56L氯气时,刚好使溶液中Fe2+完全转化为Fe3+。则该氧化物的化学式是()A












