高铁酸钾(K2FeO4)是一种集氧化 吸附 絮凝 杀菌 灭菌 去浊 脱色 除臭为一体的新型 高效 绿
| 高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝、杀菌、灭菌、去浊、脱色、除臭为一体的新型、高效、绿色环保的多功能水处理剂.近十几年来,我国对高铁酸钾在饮用水处理中的应用的研究也不断深入,已取得可喜成果.比较理想的制备方法是次氯酸盐氧化法:先向KOH溶液中通入足量Cl2制备次氯酸钾饱和溶液,再分次加入KOH固体,得到次氯酸钾强碱性饱和溶液,加入三价铁盐,合成高铁酸钾. (1)向次氯酸钾强碱饱和溶液中加入三价铁盐发生反应的离子方程式: ①Fe3++3OH-=Fe(OH);②______. (2)高铁酸钾溶于水能释放大量的原子氧,从而非常有效地杀灭水中的病菌和病毒,与此同时,自身被还原成新生态的Fe(OH)3,这是一种品质优良的无机絮凝剂,能高效地除去水中的微细悬浮物.将适量K2Fe2O4溶液于pH=4.74的溶液中,配制成c(FeO2-4)=1.0mmol?L-1试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(FeO+2-4)的变化,结果见图.高铁酸钾与水反应的离子反应方程式为______,该反应的△H______0(填“>”“<”或“=”). (3)高铁酸盐还是一类环保型高性能电池的材料,用它做成的电池能量高,放电电流大,能长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O
(4)测定某K2FeO4溶液浓度的实验步骤如下: 步骤1:准确量取V mL K2FeO4溶液加入到锥形瓶中 步骤2:在强碱性溶液中,用过量CrO-2与FeO2-4反应生成Fe(OH)3和CrO2-4 步骤3:加足量稀硫酸,使CrO2-4转化为Cr2O2-7,CrO-2转化为Cr3+,Fe(OH)3转化为Fe2+ 步骤4:加入二苯胺磺酸钠作指示剂,用c mol?L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗(NH4)2Fe(SO4)2溶液V1mL. ①滴定时发生反应的离子方程式为______. ②原溶液中K2FeO4的浓度为______(用含字母的代数式表示). 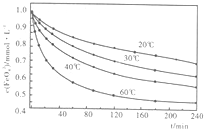 |
参考解答
| (1)次氯酸钾具有强的氧化性,和氢氧化铁之间的反应为:2Fe(OH)3+3ClO-+10OH-=2FeO2-4+3Cl-+5H2O,故答案为:2Fe(OH)3+3ClO-+10OH-=2FeO2-4+3Cl-+5H2O; (2)高铁酸钾溶于水能释放大量的原子氧,即生成氧气单质,与此同时,自身被还原成新生态的Fe(OH)3,反应为:4FeO42-+10H2O=4Fe(OH)3+8OH-+3O2↑,根据图象可以看出:随着反应的进行,反应体系的温度逐渐降低,所以反应是吸热反应,故答案为:4FeO42-+10H2O=4Fe(OH)3+8OH-+3O2↑;>; (3)该电池放电时属于原电池的工作原理,在原电池中,负极发生失电子的氧化反应,即Zn+2OH--2e-=Zn(OH),正极上发生反应为:2K2FeO4+8H2O+6e-→2Fe(OH)3+6OH-,根据正极反应,若外电路有5.418×1022个即0.09mol电子通过时,参与反应的高铁酸钾的质量为:
(4)①滴定时,Cr2O72-具有很强的氧化性,能将亚铁离子氧化为三价铁离子,发生反应的离子方程式为:6Fe2++Cr2O2-7+14H+=6Fe3++2Cr3++7H2O, 故答案为:6Fe2++Cr2O2-7+14H+=6Fe3++2Cr3++7H2O; ②在强碱性溶液中,用过量CrO-2与FeO2-4反应生成Fe(OH)3和CrO42-,CrO2-+FeO42-+2H2O=Fe(OH)3↓+CrO42-+OH-,滴定时,发生反应的离子方程式为:6Fe2++Cr2O2-7+14H+=6Fe3++2Cr3++7H2O,根据K2FeO4溶液和(NH4)2Fe(SO4)2标准溶液量的关系,可得出原溶液中K2FeO4的浓度为
|
相似问题
在MnO2+4HCl=MnC12+C12↑+2H2O的反应中:①______是氧化剂②发生氧化反应的
在MnO2+4HCl=MnC12+C12↑+2H2O的反应中:①______是氧化剂②发生氧化反应的物质是______.③在参加反应的盐酸中.起还原剂作用的HC1与起酸性作用的HC1的
阿波罗宇宙飞船以N2H4(联氨)和N2O4为动力源 反应温度达27000C 反应化学方程式为 2N2
阿波罗宇宙飞船以N2H4(联氨)和N2O4为动力源,反应温度达27000C,反应化学方程式为2N2H4+N2O4=3N2+4H2O,下列关于该反应的叙述正确的是( )A.属于
我们用字母L M Q R X分别代表五种含不同化合价的氮元素的物质 并且每种物质中氮元素的化合价只有
我们用字母L、M、Q、R、X分别代表五种含不同化合价的氮元素的物质,并且每种物质中氮元素的化合价只有一种.又知道物质L中氮元素的化合价要比物质M中氮元
实验室常用的浓盐酸物质的量浓度约为12.0mol?L-1.(1)实验室欲用上述浓盐酸配制480mL
实验室常用的浓盐酸物质的量浓度约为12 0mol?L-1.(1)实验室欲用上述浓盐酸配制480mL0 20mol?L-1的稀盐酸溶液,则需要取上述浓盐酸______mL.(2)配制
下列关于氧化还原反应的叙述正确的是( )A.氧化还原反应中 非金属元素的原子一定得电子被还原B.由
下列关于氧化还原反应的叙述正确的是( )A.氧化还原反应中,非金属元素的原子一定得电子被还原B.由H2O2→O2的过程一定需加入氧化剂才能实现C.置换












