(12分)【化学——物质结构与性质】氮族元素包括N P As Sb和Bi五种元素。(1)下列关于氮族
| (12分)【化学——物质结构与性质】 氮族元素包括N、P、As、Sb和Bi五种元素。 (1)下列关于氮族元素的说法正确的是 。
(3)PCl3分子中,Cl-P-Cl键的键角____ 109o28’(填“>”“<”或“=”)。 (4)白磷(P4)是磷的一种单质,它属于分子晶体,其晶胞结构如图。己知该晶体的密度为 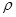 g·cm-3,晶胞的边长为acm,则阿伏加德罗常数为__ mol-l(用含ρ、a的式子表示)。 g·cm-3,晶胞的边长为acm,则阿伏加德罗常数为__ mol-l(用含ρ、a的式子表示)。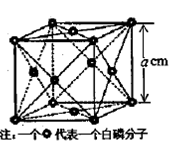 |
参考解答
| (12分) (1)b(2分) (2)NH3分子与水分子之间能够形成氢键(2分) 离子键(2分) 配位键(2分) (3) < (2分) (4)496/(ρa3) (2分) |
试题分析:(1)a、以光的形式释放能量时,电子从能量较高的轨道跃迁到能量较低的轨道,错误;b、P为第VA族元素,3p轨道排布3个电子,为半充满状态,更稳定,第一电离能较大,所以P、Na、S三种元素的第一电离能由大到小的顺序是:P>S>Na,正确;c、基态As原子中,电子占据的最高能级为4p,错误;d、Bi为第六周期第VA族元素,原子中最外层有3个能量相同的电子,错误。 (2)N、O原子半径小而电负性大,NH3分子与水分子之间能够形成氢键,PH3分子与水分子之间不能形成氢键,所以NH3在水中的溶解度比PH3大得多;[Cu(NH3)42+与SO42-之间形成了离子键;Cu2+与NH3之间形成了配位键。 (3)PCl3中P原子杂化方式为sp3杂化,分子构型为三角锥型,P原子含有一对孤对电子,对成键电子有较强的排斥作用,所以Cl-P-Cl键的键角<109o28’。 (4)根据晶胞示意图,P4分子位于晶胞的8个顶点和6个面的面心,则1个晶胞含P4分子:8×1/8+6×1/2=4,以1个晶胞为研究对象,ρ=4×124÷NA÷a3,解得NA=496/(ρa3)。 |
相似问题
几种短周期元素的原子半径及主要化合价如下表 相关说法正确的是元素代号LMXRT原子半径/nm0.16
几种短周期元素的原子半径及主要化合价如下表,相关说法正确的是元素代号LMXRT原子半径 nm0 1600 1430 1020 0890 074主要化合价+2+3+6、-2+2-2A.离子
X Y Z W四种短周期元素的最外层电子数之和为24 它们在元素周期表中的位置如下图所示 下列说法一
X、Y、Z、W四种短周期元素的最外层电子数之和为24,它们在元素周期表中的位置如下图所示,下列说法一定正确的是A.X、Y、Z的含氧酸的酸性依次增强B.W元
下列各组原子中 化学性质一定相似的是A.原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s
下列各组原子中,化学性质一定相似的是A.原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子B.原子核外M层上仅有两个电子的X原子与原
有A B C D E五种短周期的主族元素 其原子序数依次增大.其中只有C是金属 D的单质是黄色固体
有A、B、C、D、E五种短周期的主族元素,其原子序数依次增大.其中只有C是金属,D的单质是黄色固体,A、B、D在周期表中的相对位置关系如题6图.下列说法正
短周期元素W X Y Z的原子序数依次增大 W与Y原子的最外层电子数之和为X原子的最外层电子数的2倍
短周期元素W、X、Y、Z的原子序数依次增大,W与Y原子的最外层电子数之和为X原子的最外层电子数的2倍,Z原子的最外层电子数等于其最内层电子数,X、Y、Z的












