(7分)在活动探究课上 老师拿来一包由氯化钠 碳酸钠 碳酸氢钠三种物质中取出的两种物质等质量混合而成
(7分)在活动探究课上,老师拿来一包由氯化钠、碳酸钠、碳酸氢钠三种物质中取出的两种物质等质量混合而成的白色粉末和一瓶没有标签的未知酸溶液,请各实验小组同学进行成分确定。甲小组同学查阅课本后设计了如下实验方案: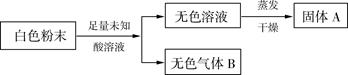
(1)写出物质名称:B ,未知酸溶液 。 (2)这包白色粉末的组成可能是 ;有关反应的化学方程式为 。 (3)若乙小组的同学取10g白色粉末也按照甲组同学的方案进行实验,他们最终得到固体的质量为8.5g。你认为这包白色粉末的组成可能是 。 |
参考解答
| (1)二氧化碳 盐酸 (2)NaCl和Na2CO3、NaCl和NaHCO3、Na2CO3和NaHCO3 Na2CO3 + 2HCl =' 2NaCl' + H2O + CO2↑,NaHCO3 + HCl=' NaCl' + H2O + CO2↑ (3)NaCl和NaHCO3 Na2CO3和NaHCO3 |
试题分析:(1)由于无色气体B能使澄清石灰水变浑浊,故B是二氧化碳;而A为人的正常生理活动所必须不可少的物质,且根据图示可知,白色粉末(氯化钠、碳酸钠、碳酸氢钠三种物质中的两种物质)和某酸反应生成A溶液和二氧化碳气体,根据质量守恒定律(元素种类不变)可知,A含有钠元素,从而可确定A为氯化钠,所以无色溶液是氯化钠溶液;故未知酸溶液中含有氯离子,则可推断未知酸溶液为稀盐酸。 (2)因为白色粉末(氯化钠、碳酸钠、碳酸氢钠三种物质中的两种物质)和稀盐酸反应有二氧化碳生成,由此可推断白色粉末中含有碳酸根离子或碳酸氢根离子;且由于白色粉末和稀盐酸反应生成氯化钠溶液,因此该白色粉末可能的组成为:NaCl和Na2CO3、NaCl和NaHCO3、Na2CO3和NaHCO3;故反应的化学方程式分别为Na2CO3+2HCl=2NaCl+H2O+CO2↑,NaHCO3+HCl=NaCl+H2O+CO2↑。 (4)8.5gNaCl中钠元素的质量=8.5g× 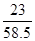 ×100%=3.34g,根据化学变化前后钠元素质量不变,则10g白色粉中钠质量的分数= ×100%=3.34g,根据化学变化前后钠元素质量不变,则10g白色粉中钠质量的分数=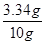 ×100%=33.4%; ×100%=33.4%;而NaCl中钠元素质量分数= 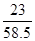 ×100%=39.3%, ×100%=39.3%,Na2CO3中钠元素质量分数= 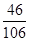 ×100%=43.3%, ×100%=43.3%,NaHCO3中钠元素质量分数= 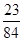 ×100%=27.4%, ×100%=27.4%,因为39.3%>33.4%>27.4%,所以白色粉末的组成为NaHCO3和NaCl; 因为43.3%>33.4%>27.4%,所以白色粉末的组成也可能为Na2CO3和NaHCO3 32-检验方法),物质的鉴别、推断,书写化学方程式 点评:本题涉及物质的推断,推断题涉及的知识点多,变化复杂,条件隐蔽,是一种既考查知识,又考查能力的题型;解题的关键是在审题的基础上找准解题的突破口,即有特征的物质或反应现象等,再根据题中的条件进行有目的假设,然后沿着假设进行推导,只要各步都满足,假设就成立。 |
相似问题
下列有关物质的检验方法和结论都合理的是A.加入盐酸 有无色气体产生的物质中一定含有碳酸盐B.用燃着的
下列有关物质的检验方法和结论都合理的是A.加入盐酸,有无色气体产生的物质中一定含有碳酸盐B.用燃着的木条伸入某气体中,火焰熄灭,则该气体一定是二
(10分)被称为“生命之源”的水和被称为“绿色氧化剂”的双氧水(过氧化氢溶液) 通常情况下均为无色液
(10分)被称为“生命之源”的水和被称为“绿色氧化剂”的双氧水(过氧化氢溶液),通常情况下均为无色液体。在化学实验开放日,实验小组的同学用下面的
A B C D四种元素 A元素组成的一种单质是自然界最硬的物质 B元素是生物细胞中含量最高的元素 C
A、B、C、D四种元素,A元素组成的一种单质是自然界最硬的物质,B元素是生物细胞中含量最高的元素,C元素原子核内只含一个质子,D+离子核外有10个电子。则
下图是常见物质转化关系图(个别产物可能略去) 其中A B常温下均为液态 且组成元素相同;Y为氧化物
下图是常见物质转化关系图(个别产物可能略去),其中A、B常温下均为液态,且组成元素相同;Y为氧化物,Z是紫红色固体。(1)在反应①中,物质X起的可能
梳理化学知识有利于理解和记忆 使你的学习更轻松。以下内容完全正确的一组是 A物质的性质与用途 B安
梳理化学知识有利于理解和记忆,使你的学习更轻松。以下内容完全正确的一组是A物质的性质与用途B安全常识乙醇具有可燃性——可作燃料N2性质稳定——可作












