(10分)如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系 已知B C D E是非金属单质
(10分)如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金属单质,且在常温常压下都是气体;化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①是化工生产中的一种重要的固氮反应。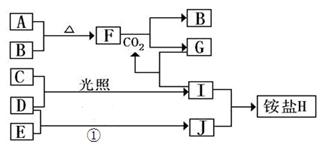 (1)单质E的结构式_____________ (2)F和H2O反应的化学方程式为_____________________________,该反应中被氧化与被还原的物质的物质的量之比是_________________ (3)铵盐H中阳离子的电子式_______________,检验H 中阳离子的方法是____________________ _____________________________________________________________________________ |
参考解答
| (1)N≡N (2)2Na2O2+2H2O=4NaOH+O2↑ ; 1:1 (3) 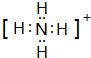 ;取少量H样品放入试管中,加入NaOH溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明含有NH4+ ;取少量H样品放入试管中,加入NaOH溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明含有NH4+ |
试题分析:化合物G的焰色反应为黄色,含有Na元素,F能与二氧化碳反应得到气体单质B与G,可推知F为Na2O2,B为O2,G为Na2CO3,而A与B(氧气)反应得到F(过氧化钠),则A为Na.G(Na2CO3)与I反应得到CO2,则I属于酸,I由气体非金属单质C与D在光照条件下得到,则I为HCl,C、D分别为H2、Cl2中的一种,I和J通常状况下呈气态,二者反应得到铵盐,且反应①是化工生产中的一种重要固氮反应,可推知J为NH3,D为H2,E为N2,铵盐H为NH4Cl,故C为Cl2; (1)单质E为N2,分子中N原子之间形成3对共用电子对,其结构式为N≡N; (2)F为过氧化钠,与H2O反应生成氢氧化钠与氧气,化学方程式为2Na2O2+2H2O=4NaOH+O2↑,该反应中被氧化与被还原的物质都是过氧化钠,由电子转移守恒可知,被氧化与被还原过氧化钠的物质的量之比是1:1; (3)铵盐H为NH4Cl,NH4+离子的电子式为 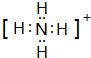 ,检验NH4+离子的方法是:取少量H 样品放入试管,加入氢氧化钠溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明有铵根离子。 ,检验NH4+离子的方法是:取少量H 样品放入试管,加入氢氧化钠溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明有铵根离子。 |
相似问题
有关物质燃烧时火焰颜色描述错误的是 [ ]A.氢气在氯气中燃烧 - 苍白色B.钠在空气中燃烧
有关物质燃烧时火焰颜色描述错误的是 [ ]A.氢气在氯气中燃烧 - 苍白色B.钠在空气中燃烧 - 黄色 C.乙醇在空气中燃烧 - 淡蓝色 D.硫在氧气中燃烧 - 绿色
将一小块钠投入盛有5mL饱和CnSO4溶液的试管里 不可能观察到的现象是( )A.钠熔成小球并在液
将一小块钠投入盛有5mL饱和CnSO4溶液的试管里,不可能观察到的现象是( )A.钠熔成小球并在液面上游动B.有气体生成C.试管底部有红色物质生成D.溶液变浑浊
已知:2[NaAl(OH)4]+CO2→2Al(OH)3↓+Na2CO3+H2O。向含2molNaO
已知:2[NaAl(OH)4]+CO2→2Al(OH)3↓+Na2CO3+H2O。向含2molNaOH、1molBa(OH)2、2mol[NaAl(OH)4]的混合液中慢慢通入CO2,则通入CO2的量和生成沉淀的量
把2.1 g CO与H2组成的混合气体与足量的O2充分燃烧后 立即通入足量的Na2O2固体中 固体的
把2.1 g CO与H2组成的混合气体与足量的O2充分燃烧后,立即通入足量的Na2O2固体中,固体的质量增加()A.2.1 gB.3.6 gC.7.2 gD.无法确定
下列物质都具有漂白作用 其中漂白原理没有利用物质化学性质的是A.过氧化钠B.二氧化硫C.次氯酸D.活
下列物质都具有漂白作用,其中漂白原理没有利用物质化学性质的是A.过氧化钠B.二氧化硫C.次氯酸D.活性炭












