现有下列四组溶液 每组包括三种溶液并按A B C顺序排列:甲 乙
| 现有下列四组溶液,每组包括三种溶液并按A、B、C顺序排列: 甲 乙 丙 丁 A.BaCl2 Na2CO3 KCl K2CO3 B.硝酸 硝酸 盐酸 盐酸 C.Na2CO3 AgNO3 K2CO3 BaCl2 请根据下列操作中所观察的现象完成下列问题: 向CaCl2溶液中加入A溶液产生白色沉淀;继续加入过量的B溶液沉淀消失,并产生无色无味的气体;再加入少量的C溶液,又生成白色沉淀。 (1)上述操作过程中,选用了 组溶液。 (2)有关反应的离子方程式是 。 |
参考解答
| (1)乙 (2)Ca2++CO 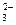  CaCO3↓ CaCO3↓CaCO3+2H+  Ca2++CO2↑+H2O Ca2++CO2↑+H2OAg++Cl-  AgCl↓ AgCl↓ |
向CaCl2溶液中加入A产生白色沉淀,四组溶液中乙、丁均产生CaCO3沉淀,继续加入过量B溶液,乙、丁均符合;再加入少量C溶液,又生成白色沉淀,则只有乙符合;因加入C之前,溶液中含有Cl-,与加入的Ag+反应产生AgCl沉淀。而丁不符合,因溶液中不含与Ba2+结合成沉淀的CO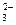 。 。 |
相似问题
有两个无标签的试剂瓶 分别盛有Na2CO3 NaHCO3固体 有四位同学为鉴别它们采用了以下不同方法
有两个无标签的试剂瓶,分别盛有Na2CO3、NaHCO3固体,有四位同学为鉴别它们采用了以下不同方法,其中可行的是A.分别将它们配制成溶液,再加入澄清石灰水
将小块金属钠投入滴有酚酞的水中 不可能出现的现象是 ( )A.钠浮
将小块金属钠投入滴有酚酞的水中,不可能出现的现象是()A.钠浮在水面上B.熔化成一个小球C.产生沉淀D.溶液变红
加热3.24 g碳酸钠和碳酸氢钠的混合物至质量不再变化 剩余固体的质量为2.51 g。计算原混合物中
加热3 24 g碳酸钠和碳酸氢钠的混合物至质量不再变化,剩余固体的质量为2 51 g。计算原混合物中碳酸钠的质量分数。
可以用来鉴别Na2CO3溶液和NaHCO3溶液最好的是A.加CaCl2溶液B.加热C.加稀盐酸D.加
可以用来鉴别Na2CO3溶液和NaHCO3溶液最好的是A.加CaCl2溶液B.加热C.加稀盐酸D.加澄清的石灰水
关于锂 钠 钾 铷 铯的性质递变规律 不正确的叙述是A.单质的密度依次增大B.单质的熔沸点依次降低C
关于锂、钠、钾、铷、铯的性质递变规律,不正确的叙述是A.单质的密度依次增大B.单质的熔沸点依次降低C.单质的还原性依次增强D.离子的氧化性依次减弱












