为探究CO2的化学性质 需要制取并收集干燥的CO2 以下是老师提供的一些实验装置。 (1)实验室制取
为探究CO2的化学性质,需要制取并收集干燥的CO2,以下是老师提供的一些实验装置。 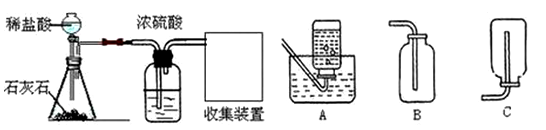 (1)实验室制取CO2的化学方程式为_ _; (2)浓硫酸的作用是____ __,收集装置为__ _(填字母); (3)学校实验室的废液缸中收集了同学们在实验室制取二氧化碳的废液。小溪同学想探究废液中溶质的成分,请你共同参与探究,并回答下列问题: 【提出问题]】废液中的溶质是什么物质? 【做出猜想】小溪认为废液中溶质只有氯化钙。 你认为还可能含有的溶质是 (填化学式); 【查阅资料】氯化钙溶液呈中性。 【实验与结论】 ①小溪分别取少量该废液和氯化钙溶液加入到两支试管中,并向其中分别滴入无色酚酞试液作对比实验,结果两支试管中溶液均为无色,于是小溪认为自己的猜想是正确的。 ②你认为小溪的实验 (填“能”或“不能”)证明她的猜想,理由是 。 ③如果要证明你的猜想是正确的,你选择的试剂是 ,试验中可以看到的实验现象是 。 【拓展与应用】 ①若实验证明你的猜想是正确的,要想使处理后的废液只有氯化钙溶液,应向废液中加入过量的 ,反应完成后静置过滤,得到纯净的氯化钙溶液。 ②通过以上探究,你认为实验室的废液未经处理直接倒入下水道,可能造成的危害是 。(写一条) |
参考解答
| (1)CaCO3+2HCl===CaCl2+H2O+CO2↑(2分) (2)干燥二氧化碳气体(1分) B(1分) (3)【做出猜想】HCl(1分)【实验与结论】②不能(1分)酚酞遇盐酸也不变色,无法确定是否含有HCl(1分)③紫色石蕊试液或碳酸钠溶液或较活泼的金属(1分) 溶液变红或产生气泡等合理答案(1分) 【拓展与应用】①石灰石(或CaCO3粉末)等(1分)②可能腐蚀管道或者污染水质等。(1分) |
| 分析:实验室是用石灰石和稀盐酸来制取二氧化碳的,二氧化碳的密度比空气的密度大,能溶于水,因此只能用向上排空气法收集气体,反应后的溶液中除了生成的氯化钙之外,还可能有剩余的盐酸.要证明盐酸的存在可利用酸的化学性质进行分析. 解答:解:(1)实验室制取CO2的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑ (2)浓硫酸具有吸水性,能干燥二氧化碳气体,二氧化碳密度比空气大,能溶于水,只能用向上排空气法收集. (3)盐酸和大理石反应时盐酸可能有剩余,故猜想溶质为HCl,要证明盐酸剩余,即证明溶液呈酸性可利用酸的化学性质,因此可用紫色石蕊试液或碳酸钠溶液或较活泼的金属,现象为溶液变红或产生气泡.小溪利用无色酚酞试液证明溶液呈酸性是错误的,酚酞在酸性或中性溶液中都不变色. 【拓展与应用】 要想将溶液中的氯化氢去掉,处理后的废液只有氯化钙溶液,则加入的物质与盐酸反应生成物中只能有氯化钙溶解在水中,因此要加入不溶性的碳酸钙或石灰石.如果呈酸性的废液倒入下水道,会可能腐蚀管道或者污染水质等 故答案为:(1)CaCO3+2HCl═CaCl2+H2O+CO2↑; (2)干燥二氧化碳气体 B; 【做出猜想】HCl; 【实验与结论】②不能;酚酞遇盐酸也不变色,无法确定是否含有HCl; ③紫色石蕊试液或碳酸钠溶液或较活泼的金属; 溶液变红或产生气泡等合理答案; 【拓展与应用】①石灰石(或CaCO3粉末)等;②可能腐蚀管道或者污染水质等. |
相似问题
(8分)某化学兴趣小组的同学进行木炭还原氧化铜的探究实验;生成物是红色固体和无色气体。他们通过查阅资
(8分)某化学兴趣小组的同学进行木炭还原氧化铜的探究实验;生成物是红色固体和无色气体。他们通过查阅资料后,得知氧化亚铜(Cu2O)为红色固体,因此猜想生
利用家庭生活用品也可以对化学进行学习和实验探究活动。下列实验仅利用家庭生活用品不可能完成的是 A
利用家庭生活用品也可以对化学进行学习和实验探究活动。下列实验仅利用家庭生活用品不可能完成的是A.蛋白质在加热条件下失去生理活性B.检验豆油中是否
乙炔(化学式C2H2)俗称电石气 实验室中常用电石(一种灰色块状固体 化学式CaC2)与水在常温下反
乙炔(化学式C2H2)俗称电石气,实验室中常用电石(一种灰色块状固体,化学式CaC2)与水在常温下反应制取,该反应中同时还有氢氧化钙[Ca(OH)2]生成.通
如图是实验室制取气体时常用的装置请按要求填空(填装置的字母代号):(1)制取并用排水法收集氧气应选用
如图是实验室制取气体时常用的装置请按要求填空(填装置的字母代号):(1)制取并用排水法收集氧气应选用的装置是______.(2)制取并收集二氧化碳气体
下列气体中 前者只能用排水法收集 后者只能用向上排空气法收集的是( )A.O2 H2B.O2 CO
下列气体中,前者只能用排水法收集,后者只能用向上排空气法收集的是( )A.O2,H2B.O2,CO2C.CO,CO2D.CO,H2












