下图所示装置中 甲 乙 丙三个烧杯依次分别盛放100g5.00%的NaOH溶液 足量的CuSO4溶液
| 下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极。 |
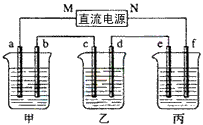 |
| (1)接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。 据此回答问题: ① 电源的N端为___________极; ② 电极b上发生的电极反应为___________; ③ 列式计算电极b上生成的气体在标准状况下的体积:___________; ④ 电极c的质量变化是___________g; ⑤ 电解前后个溶液的酸、碱性大小是否发生变化,简述其原因: 甲溶液____________________;乙溶液___________________;丙溶液______________________; (2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么?____________________________________________。 |
参考解答
| (1)①正极;②4OH--4e-==2H2O+O2↑;③2.8L;④16g;⑤甲增大,因为相当于电解水;乙减小,OH- 放电,H+增多;丙不变,相当于电解水 (2)可以,因为CuSO4溶液已转变为H2SO4溶液,反应也就变为水的电解反应 |
相似问题
用惰性电极实现电解 下列说法正确的是[ ]A.电解稀硫酸溶液 实质上是电解水 故溶液pH不变
用惰性电极实现电解,下列说法正确的是[ ]A.电解稀硫酸溶液,实质上是电解水,故溶液pH不变 B.电解稀氢氧化钠溶液,要消耗OH-,故溶液pH减小 C.电
市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作
市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子
金属镍有广泛的用途 粗镍中含有少量Fe Zn Cu Pt等杂质 可用电解法制备高纯度的镍 下列叙述正
金属镍有广泛的用途,粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性Fe2+)[ ]A.阳极发生还原反应,其
甲醇是一种可再生能源 具有开发和应用的广阔前景 工业上一般可采用如下反应来合成甲醇:CO(g)+2H
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)CH3OH(g),现在实验室模拟该反应并进行分析。(1)
下图是电解CuCl2溶液的装置 其中c d 为石墨电极。则下列有关的判断正确的是[ ]A.a
下图是电解CuCl2溶液的装置,其中c、d 为石墨电极。则下列有关的判断正确的是[ ]A.a为负极、b为正极 B.a为阳极、b为阴极 C.电解过程中、d电极质量












