已知CO2 BF3分别为直线形 V形和平面三角形。试用等电子原理说明下列分子或离子的成键情况和几何
已知CO2、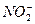 、BF3分别为直线形、V形和平面三角形。试用等电子原理说明下列分子或离子的成键情况和几何构型。 、BF3分别为直线形、V形和平面三角形。试用等电子原理说明下列分子或离子的成键情况和几何构型。O3、 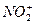 、 、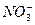 、 、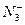 、 、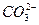 |
参考解答
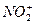 、 、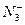 为直线形,O3为V形, 为直线形,O3为V形,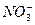 、 、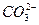 为平面三角形。 为平面三角形。 |
根据等电子原理,原子数相同的分子或离子中,若电子数也相同,则这些分子或离子具有相似的电子结构和相似的几何构型。将各分子或离子的电子总数算出来,分别与CO2,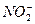 ,BF3对照,即可得出其电子结构和几何构型: ,BF3对照,即可得出其电子结构和几何构型:CO2、 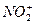 、 、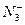 为等电子体,均为直线形; 为等电子体,均为直线形;O3、 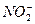 为等电子体,均为V形; 为等电子体,均为V形;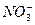 、 、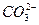 与BF3为等电子体,均为平面三角形。 与BF3为等电子体,均为平面三角形。 |
相似问题
已知[Co(NH3)6]3+呈正八面体结构 若其中有两个NH3分子分别被Cl-和H2O取代 所形成的
已知[Co(NH3)6]3+呈正八面体结构,若其中有两个NH3分子分别被Cl-和H2O取代,所形成的[Co(NH3)2Cl2(H2O)2]3+的几何异构体种数有(不考虑光学异构)几种( )A.3种B.4种C.5种D.6种
已知六氟化硫分子呈正八面体 具有很好的绝缘性 即使在高电压下熔融也不导电 在电器行业有着广泛用途 但
已知六氟化硫分子呈正八面体,具有很好的绝缘性,即使在高电压下熔融也不导电,在电器行业有着广泛用途,但其沸点较低,逸散到空气中会引起温室效应。下
下列说法中正确的是A.在离子化合物里 只存在离子键 没有共价键B.非极性键只存在于双原子的单质分子中
下列说法中正确的是A.在离子化合物里,只存在离子键,没有共价键B.非极性键只存在于双原子的单质分子中C.共价化合物中只有共价键,一定没有离子键D.
下列的叙述中不正确的是( )A.卤化氢分子中 卤素的非金属性越强 共价键的极性越强 稳定性也越强B.
下列的叙述中不正确的是( )A.卤化氢分子中,卤素的非金属性越强,共价键的极性越强,稳定性也越强B.以非极性键结合的分子,不一定是非极性分子C.判
(10分)乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。(1)CaC2中C22—
(10分)乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。(1)CaC2中C22—与O22+互为等电子体,O22+的电子式可表示为______________;1












