对可逆反应:NO(g)+CO(g)?N2(g)+CO2(g) △H=-372.2KJ/mol达到平衡
对可逆反应:NO(g)+CO(g)?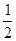 N2(g)+CO2(g) △H=-372.2KJ/mol达到平衡后,为提高该反应的反应速率和NO的转化率,以下采取的措施正确的是( ) N2(g)+CO2(g) △H=-372.2KJ/mol达到平衡后,为提高该反应的反应速率和NO的转化率,以下采取的措施正确的是( )
|
参考解答
| C |
| A错,加催化剂平衡不移动;B错,该反应的正反应方向为放热反应,升高温度平衡将向逆反应方向移动;C正确;增大压强平衡向气体体积减少的方向移动,同时加入催化剂反应速率加快人;D错,降低温度反应速率减慢; |
相似问题
定温度 压强和有铁触媒的条件下 在密闭容器中充入N2 H2和NH3 。若起始时n(N2)='x' m
定温度、压强和有铁触媒的条件下,在密闭容器中充入N2、H2和NH3 。若起始时n(N2)="x" mol、n(H2)="y" mol、n(NH3)="z" mol (x、y、z均不为0 ),平
有关合成氨的下列叙述中 不能用勒夏特列原理解释的是A.加入催化剂能使合成氨反应速率加快B.高压有利于
有关合成氨的下列叙述中,不能用勒夏特列原理解释的是A.加入催化剂能使合成氨反应速率加快B.高压有利于提高NH3的产量C.温度过高不利于氨的生成D.增大
已知溶液中存在Cr2O72-+ H2O2CrO42-+ 2H+的平衡 其中Cr2O72-呈橙色 Cr
已知溶液中存在Cr2O72-+ H2O2CrO42-+ 2H+的平衡,其中Cr2O72-呈橙色,CrO42-呈黄色,向该平衡体系中滴加饱和NaOH溶液时,颜色的变化情况是A.黄色加
(6分)可逆反应①X(g)+2Y(g) 2Z(g) ②2M(g) N(g)+P(g)分别在密闭容器
(6分)可逆反应①X(g)+2Y(g) 2Z(g) 、②2M(g) N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到
温度体积固定的容器中建立2NO2N2O4平衡 平衡时NO2与N2O4物质的量浓度之比为Φ 条件不变的
温度体积固定的容器中建立2NO2N2O4平衡,平衡时NO2与N2O4物质的量浓度之比为Φ,条件不变的情况下,分别再充入NO2和再充入N2O4,平衡后会引起Φ的变化正












