(10分)温室效应和资源短缺等问题和如何降低大气中的CO2含量并加以开发利用引起了各国的普遍重视。目
(10分)温室效应和资源短缺 等问题和如何降低大气中的CO2含量并加以开发利用引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) 等问题和如何降低大气中的CO2含量并加以开发利用引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)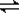 CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。 CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。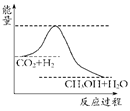 (1)关于该反应的下列说法中,正确的是________。 A.ΔH>0,ΔS>0 B.ΔH>0,ΔS<0 C.ΔH<0,ΔS<0 D.ΔH<0,ΔS>0 (2)该反应平衡常数K的表达式为________________________________。 (3)温度降低,平衡常数K________(填“增大”、“不变”或“减小”)。 (4)为探究反应原理,现进行如下实验:在体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率v(H2)________mol·L-1·min-1。 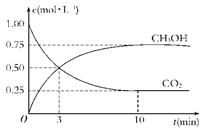 (5)下列措施中能使n(CH3OH)/n(CO2)增大的有________。 A.升高温度 B.加入催化剂 C.将H2O(g)从体系中分离 D.再充入1 mol CO2和3 mol H2 E.充入He(g),使体系总压强增大 |
参考解答
| (1)C (2) (3)增大 (4)0.225 (5)CD |
| 略 |
相似问题
如图是温度和压强对反应2Z(g)x+Y的影响示意图 图中横坐标表示温度 纵坐标表示平衡混合气体中z的
如图是温度和压强对反应2Z(g)x+Y的影响示意图,图中横坐标表示温度,纵坐标表示平衡混合气体中z的体积分数。则下列叙述正确的是A.上述可逆反应的正反
将2.0 mol SO气体和2.0 mol SO气体混合于固定体积的密闭容器中 在一定条件下发生反应
将2 0 mol SO气体和2 0 mol SO气体混合于固定体积的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g)2SO3(g),达到平衡时SO3为n mol 。在相同温度
(12分)(1)对反应N2O4(g)2NO2(g) △H>0 在温度为T1 T2时 平衡体系中N
(12分)(1)对反应N2O4(g)2NO2(g) △H>0 ,在温度为T1、 T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。T1T2(填“>”、“<”或“=”
(10分)在一定条件下 xA + yBzC 达到平衡 试填写下列空白:( 1 ) 若A B C都是气
(10分)在一定条件下,xA + yBzC,达到平衡,试填写下列空白:( 1 ) 若A、B、C都是气体,减压后向逆反应方向移动,则x、y、x之间的关系是 。(
(12分)随着氮氧化物污染的日趋严重 国家将于“十二五”期间加大对氮氧化物排放的控制力度。目前 用活
(12分)随着氮氧化物污染的日趋严重,国家将于“十二五”期间加大对氮氧化物排放的控制力度。目前,用活性炭还原法处理氮氧化物是消除氮氧化物污染的有效












