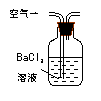
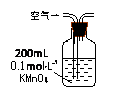
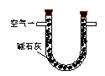
Ⅰ.(1)某兴趣小组甲设计了以下装置和方法测定空气中SO2含量。你认为可行的操作是
Ⅰ.(1)某兴趣小组甲设计了以下装置和方法测定空气中SO2含量。你认为可行的操作是 (填序号)
(2)兴趣小组乙取336mL(标准状况)某由SO2和N2组成的混合气体Y,将其通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由此推知气体Y中SO2的体积分数为 。 Ⅱ某化学兴趣小组丙为探究Fe3+是否能氧化SO2,设计了如下实验装置。 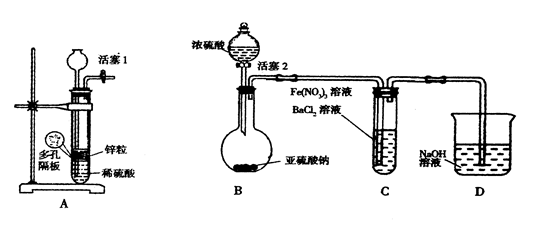 (1)如上图连接好装置。实验前应进行 操作 (2)观察到装置C中产生了白色沉淀,同学们提出了以下猜想(每个猜想只考虑一种物质的氧化性)。 猜想1: ; 猜想2:SO2被Fe3+氧化了; 猜想3:SO2被NO3—氧化了 (3)甲同学认为猜想1正确,并利用上述装置A进行了排除干扰的探究实验。 (4)乙同学认为猜想2正确,则装置C中反应的离子方程式是 (5)丙同学认为猜想3正确,他利用甲同学的实验装置,设计实验验证猜想。请在答题卡上写出实验步骤以及预期现象和结论。限选实验试剂:NaNO3溶液、KSCN溶液、FeCl3溶液、BaCl2溶液、
Fe(NO3)3溶液 |
参考解答
| Ⅰ(1)B (2)66.7% Ⅱ(1)检查装置的气密性 (2)空气与SO2进入H2O中,生成了H2SO4 (4)SO2 + 2Fe3+ + Ba2+ + 2H2O=BaSO4↓+ 2Fe2+ + 4H+ (5)
|
试题分析:Ⅰ.(1)A中通入二氧化硫气体不会生成沉淀,故错误。B中二氧化硫和高锰酸钾反应生成了硫酸根,紫色褪色,可以检测,正确;空气中含有二氧化碳也会与碱石灰反应,错误;(2)兴趣小组乙取336mL(标准状况)某由SO2和N2组成的混合气体Y,将其通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由此推知气体Y中SO2的体积分数为SO2具有还原性,通入足量溴水中,发生SO2+Br2+2H2O=2HBr+H2SO4,离子方程式的书写,将产物中的氢溴酸和硫酸拆成离子,所以离子方程式为SO2+Br2+2H2O═2Br-+SO42-+4H+,生成的硫酸遇到氯化钡会产生白色沉淀,可以先洗涤然后再过滤来获得纯净的硫酸钡沉淀,则n(混合气体)=0.336L/22.4=0.015mol,  则 SO2的体积分数:0.01/0.015=66.7%。(1)如上图连接好装置。实验前应进行检查装置的气密性 操作。 则 SO2的体积分数:0.01/0.015=66.7%。(1)如上图连接好装置。实验前应进行检查装置的气密性 操作。(2)根据可会把SO2氧化为正6价的硫,还有可能是空气中的氧气,故猜想1: 空气与SO2进入H2O中,生成了H2SO4。 (3)甲同学认为猜想1正确,并利用上述装置A进行了排除干扰的探究实验。 (4)根据氧化还原反应原理,由于三价铁离子有强氧化性能把二氧化硫转化为硫酸根离子,则装置C中反应的离子方程式是SO2 + 2Fe3+ + Ba2+ + 2H2O=BaSO4↓+ 2Fe2+ + 4H+ 。 (5)只要把三价铁离子不要引入这样就会避免干扰就行,故可选实验试剂:NaNO3溶液BaCl2溶液进行实验,将装置C中的溶液换为NaNO3和BaCl2的混合溶液,然后打开分液漏斗活塞进行反应。反应一段时间后,若C中出现白色沉淀,则证明猜想3正确。 |
相似问题
六水氯化锶(SrCl2·6H2O)是实验室重要的分析试剂 工业上常以天青石(主成分为SrSO4)为原
六水氯化锶(SrCl2·6H2O)是实验室重要的分析试剂,工业上常以天青石(主成分为SrSO4)为原料制备,生产流程如下:(1)第①步反应前天青石先研磨粉碎,
从碘的四氯化碳溶液中除去碘以回收四氯化碳 下列操作最简便的是A.向其中放入过量镁条 反应完毕后取出B
从碘的四氯化碳溶液中除去碘以回收四氯化碳,下列操作最简便的是A.向其中放入过量镁条,反应完毕后取出B.蒸馏 C.加入能氧化I2的KMnO4,再分液D.通入氯气
以下是对某溶液进行离子检验的方法和结论 其中正确的是( )A.先加入BaCl2溶液 再加入HNO3
以下是对某溶液进行离子检验的方法和结论,其中正确的是()A.先加入BaCl2溶液,再加入HNO3溶液,产生了白色沉淀,则溶液中一定含有大量的SO42-B.加入
下列实验做法不正确的是A.用无水硫酸铜检验乙醇中是否含水B.用溴水检验汽油中是否含有不饱和脂肪烃C.
下列实验做法不正确的是A.用无水硫酸铜检验乙醇中是否含水B.用溴水检验汽油中是否含有不饱和脂肪烃C.用蒸馏的方法可以分离醋酸与乙醇的混合物D.检验
某研究性学习小组拟探究在含Mg2+ Al3+ 的混合溶液中滴加NaOH溶液时 生成氢氧化物沉淀的过程
某研究性学习小组拟探究在含Mg2+、Al3+ 的混合溶液中滴加NaOH溶液时,生成氢氧化物沉淀的过程。【实验】在0 1 mol?L-1 MgSO4、0 05 mol?L-1Al2(SO4