(13分)某课外活动小组加热炭粉(过量)和氧化铜的混合物 再用下图装置 对获得的铜粉(含炭)样品进行
(13分)某课外活动小组加热炭粉(过量)和氧化铜的混合物,再用下图装置,对获得的铜粉(含炭)样品进行实验。图中铁架台等装置已略去。请你帮助他们完成下列实验报告。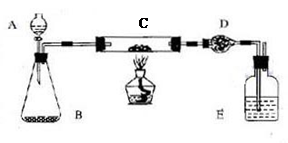 (一)实验目的:__________________________________。 (二)实验用品:仪器:天平、分液漏斗、锥形瓶、硬玻璃管、干燥管、酒精灯、洗气瓶等 药品:红褐色铜粉(含炭)样品、过氧化钠、碱石灰、水、浓硫酸等 (三)实验内容:
(五)问题和讨论: 实验完成后,老师评议说:按上述实验设计,即使C中反应完全、D中吸收完全,也不会得出正确的结果。经讨论,有同学提出在B与C之间加入一个装置。再次实验后,得到了较正确的结果。那么,原来实验所测得的铜的质量分数偏小的原因可能是_______________,在B与C之间加入的装置可以是___________,其中盛放的药品是__________________。 |
参考解答
| (一)测定铜粉样品中铜的质量分数 (2分) (三)
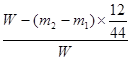 (2分) (2分)(五)水蒸汽通过C被D中碱石灰吸收 (2分) 洗气瓶 浓硫酸 (或干燥管 碱石灰) (各1分 共2分) |
试题分析::(一)由实验装置流程图可以看了B装置是过氧化钠制氧气,C装置是铜和碳分别与氧气反应,碳转化成二氧化碳被D装置吸收,D装置增重的质量就是生成的二氧化碳的质量,由此可计算出样品的碳的质量,从而求出样品中铜的质量分数 (三)B中是过氧化钠制氧气,因此BE中看到的现象是有气泡产生。C中铜与氧气在加热条件下生成氧化铜,C与氧气在点燃条件下生成二氧化碳,因此可看到C中红色粉末变成黑色。 (四)D装置增重的质量即二氧化碳的质量为m2-m1,二氧化碳中碳元素的质量为(m2-m1)×12/44,则样品中铜的质量分数为 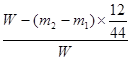 点评:首先还是要将化学反应的装置看懂,分析每个实验装置的作用,然后根据实验装置及药品分析作用,关键在于利用元素质量守恒求物质质量。 |
相似问题
鉴别某种白色织物是否是蚕丝制品 可选用的适宜方法是( )A.滴加盐酸B.滴加浓硫酸C.滴加氢
鉴别某种白色织物是否是蚕丝制品,可选用的适宜方法是( )A.滴加盐酸B.滴加浓硫酸C.滴加氢氧化钠溶液D.滴加浓硝酸
将下列物质的量浓度相等的溶液等体积两两混合有白色沉淀生成 加入过量的稀硝酸后 沉淀消失并放出气体 再
将下列物质的量浓度相等的溶液等体积两两混合有白色沉淀生成,加入过量的稀硝酸后,沉淀消失并放出气体,再加入硝酸银溶液又有白色沉淀生成的是 A.Na2CO3
下列几种情况 对中和滴定结果无影响的是( )A.滴定管用蒸馏水洗后注入标准液B.滴定管尖端未充满液
下列几种情况,对中和滴定结果无影响的是( )A.滴定管用蒸馏水洗后注入标准液B.滴定管尖端未充满液体C.滴定管中标准液在零刻度以上D.盛未知浓度溶
要除去混在石英砂中的少量碳酸钙 应采取的方法是( )A.加水溶解后 过滤分离B.加稀盐酸溶解后 过
要除去混在石英砂中的少量碳酸钙,应采取的方法是( )A.加水溶解后,过滤分离B.加稀盐酸溶解后,过滤分离C.加NaOH溶液溶解后,过滤分离D.用酒精灯加热
红葡萄酒密封储存时间越长 质量越好 原因之一是储存过程中生成了有香味的酯。在实验室也可以用如右下图所
红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯。在实验室也可以用如右下图所示的装置制取乙酸乙酯,请回答下列问题。(1)乙












