A和B两种有机物 各取0.1mol 充分燃烧 都生成4.48L CO2(标准状况)和3.6g H2O
| A和B两种有机物,各取0.1mol 充分燃烧,都生成4.48L CO2(标准状况)和3.6g H2O。已知A对氢气的相对密度为14,B中碳元素的质量分数为40%,且B的水溶液具有导电性。试求A和B的分子式,并写出它们的结构简式 |
参考解答
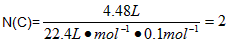 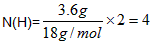 则化合物分子式为C2H4Ox M(A)=DM(H2)=14×2=28 则A为C2H4,结构简式:CH2=CH2 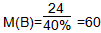 24+4+16x=60;x=2 则B为C2H4O2,依题意,B的结构简式为CH3COOH |
相似问题
将0.1mol的两种气态烃组成的混合气体 完全燃烧后得到3.36L(标准状况)CO2和3.6gH2O
将0 1mol的两种气态烃组成的混合气体,完全燃烧后得到3 36L(标准状况)CO2和3 6gH2O,下列说法正确的是 [ ]A.一定有乙烯 B.一定有甲烷 C
两种气态烃组成的混合气体0.1mol 完全燃烧得0.16molCO2和3.6g水 下列说法正确的是
两种气态烃组成的混合气体0.1mol,完全燃烧得0.16molCO2和3.6g水,下列说法正确的是 [ ]A.混合气体中一定有甲烷B.混合气体中一定是甲烷和乙烯 C
完全燃烧0.1mol某烃 燃烧产物依次通过下图所示的装置 实验结束后 称得甲装置增重9.0g 乙装置
完全燃烧0 1mol某烃,燃烧产物依次通过下图所示的装置,实验结束后,称得甲装置增重9 0g,乙装置增重17 6g 求:(1)该烃的化学式 (2)写出其所有的结
已知某烃A含碳元素的质量分数为85.7%。结合以下信息回答问题:(1)若烃A密度是相同状况下氢气密度
已知某烃A含碳元素的质量分数为85 7%。结合以下信息回答问题:(1)若烃A密度是相同状况下氢气密度的42倍。则烃A的相对分子质量_____________,分子式为
一定质量的甲烷燃烧后 得到CO CO2和水蒸气的混合气49.6g 当其缓慢经过无水CaCl2时 Ca
一定质量的甲烷燃烧后,得到CO、CO2和水蒸气的混合气49 6g,当其缓慢经过无水CaCl2时,CaCl2增重25 2g,原混合气体中CO2的质量为[ ]A.12 5 gB.13 2 g C.19 7 g D.24 4 g












