将甲烷和氧气按一定物质的量之比混合点燃后 测得生成物总质量为18.4g 将全部生成物通过足量浓硫酸后
| 将甲烷和氧气按一定物质的量之比混合点燃后,测得生成物总质量为18.4g,将全部生成物通过足量浓硫酸后,质量减少了9g。 (1)通过计算可得出原混合气体中甲烷的物质的量为___________mol。 (2)通过对(1)计算结果的进一步分析,可推知原混合气体反应后的生成物应为_____________和水组成的混合物(填化学式)。 (3)求原混合气体中甲烷和氧气的物质的量之比(写出详细的计算过程)。 |
参考解答
| (1)0.25mol (2)CO2、CO (3)解: 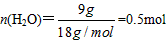 由CH4~2H2O得知,n(CH4)=n(H2O)/2=0.25mol 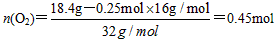 n(CH4):n(O2)=0.25mol :0.45mol=5:9 |
相似问题
将16.2g的淀粉溶于水 加入适量稀H2SO4 加热一段时间后 冷却 用碱溶液中和水解液 加入足量的
将16 2g的淀粉溶于水,加入适量稀H2SO4,加热一段时间后,冷却,用碱溶液中和水解液,加入足量的银氨溶液,水浴加热,反应完全后,得到16 2g的银,求淀粉
某种气态烃气体0.1 mol 完全燃烧得0.2molCO2和3.6gH2O 下列关于该气体的说法正确
某种气态烃气体0 1 mol,完全燃烧得0 2molCO2和3 6gH2O,下列关于该气体的说法正确的是[ ]A.乙烯B.丙烯C.甲烷 D.乙烷
有甲烷和氢气的混合气体VL 完全燃烧需要氧气的体积在相同状况下也是VL 则原混合气体中 甲烷和氢气的
有甲烷和氢气的混合气体VL,完全燃烧需要氧气的体积在相同状况下也是VL,则原混合气体中,甲烷和氢气的体积比为 [ ]A.1∶1 B.1∶2 C.
1mol某烃在氧气中充分燃烧 需要消耗氧气179.2 L(标准状况下)。它在光照的条件下与氯气反应能
1mol某烃在氧气中充分燃烧,需要消耗氧气179 2 L(标准状况下)。它在光照的条件下与氯气反应能生成3种不同的一氯取代物。该烃的结构简式是[ ]A.B.CH
现有乙酸 乙烯和丙烯(C3H6)的混合物 其中氧的质量分数为a 则碳的质量分数是[ ]A.
现有乙酸、乙烯和丙烯(C3H6)的混合物,其中氧的质量分数为a,则碳的质量分数是[ ]A. B. C. D.












