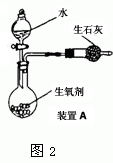
图1是一种“化学氧自救器”(又称“自生氧防毒面具”) 其使用的生氧剂(主要成分是KO2)的作用原理为
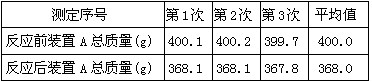
| 图1是一种“化学氧自救器”(又称“自生氧防毒面具”),其使用的生氧剂(主要成分是KO2)的作用原理为:4KO2+2CO2==2K2CO3+3O2某研究小组取100g生氧剂,放入装置A中,加入足量水与生氧剂充分反应(化学方程式为:4KO2+2H2O==4KOH+3O2↑),测定反应前后装置A的总质量,他们进行了三次实验。测定结果如下: |
|
| 请根据上述实验结果计算:(假设杂质不与水反应产生气体) (1)100g生氧剂与足量水反应生成的氧气质量; (2)生氧剂中KO2的质量分数; (3)若成人每分钟正常需氧量为0.32g,则能维持成人正常呼吸20分钟的“化学氧自救器”,至少要装入这种生氧剂多少克?[注:第(3)小题不必写出解题过程)] |
参考解答
| (1)m(O2)=400g-368g=32g; (2)94.7%; (3)14.2g |
相似问题
质量均为mg的铁和锌 分别投入到50g质量分数相同的稀硫酸中 充分反应后均产生0.2g氢气 下面结论
质量均为mg的铁和锌,分别投入到50g质量分数相同的稀硫酸中,充分反应后均产生0 2g氢气,下面结论错误的是[ ]A、锌一定无剩余 B、铁一定有剩余 C、m值
有一瓶因保存不当而部分变质的氢氧化钠固体 为测定其成分 称取10g样品配成溶液 向其中滴加溶质质量分
有一瓶因保存不当而部分变质的氢氧化钠固体,为测定其成分,称取10g样品配成溶液,向其中滴加溶质质量分数为7 3%的稀盐酸,只放出二氧化碳气体且质量与
氢氧化钠潮解后极易与二氧化碳反应而变质。为测定实验室里一瓶放置已久的烧碱中氢氧化钠的质量分数 某同学
氢氧化钠潮解后极易与二氧化碳反应而变质。为测定实验室里一瓶放置已久的烧碱中氢氧化钠的质量分数,某同学取5 3g烧碱样品放在小烧杯中,然后加入20g稀硫
实验测知久储的某NaOH固体中含有水的质量分数为3.5% 含Na2CO3的质量分数为6.5%。若取质
实验测知久储的某NaOH固体中含有水的质量分数为3 5%,含Na2CO3的质量分数为6 5%。若取质量为ag的此样品加入到含HCl质量为bg的稀盐酸(过量)中,完全反应
148mL稀盐酸(密度为1.2g/cm3) 跟50g含少量杂质的石灰石恰好完全反应(其中杂质不与盐酸
148mL稀盐酸(密度为1 2g cm3),跟50g含少量杂质的石灰石恰好完全反应(其中杂质不与盐酸反应,不与生成物反应,也不溶于水),生成17 6g气体。 计算: