现有铁粉与木炭粉混合物40克 与足量的稀硫酸反应 产生标准状况下(指0℃ 标准大气压强)气体1克 将
| 现有铁粉与木炭粉混合物40克,与足量的稀硫酸反应,产生标准状况下(指0℃、标准大气压强)气体1克,将反应后所得混合物进行过滤,得一定质量的滤渣。请计算: (1)原混合物中炭粉的质量分数。 (2)将全部滤渣溶在浓硫酸中,发现其完全溶解,并放出刺激性气味气体,发生的化学议程式为:C+2H2SO4(浓、热)==CO2↑+2SO2↑+2H2O,求理论上此滤渣与热的浓硫酸反应产生的气体总质量为多少克(标准状况下,且有害气体最后集中处理)? |
参考解答
| 解:(1)设原混合物中铁的质量为X Fe+H2SO4==FeSO4+H2↑ 56 2 X 1g 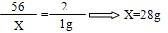 则炭粉的质量分数为: 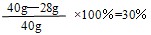 (2)设全部炭粉与热的浓H2SO4反应产生CO2、SO2气体的质量分别为y和z。 C+2H2SO4=CO2↑+2SO2↑+2H2O 12 44 2×64 12g y z 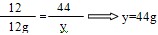 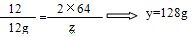 产生气体的总质量为:44g+128g=172g 答:设原混合物中铁的质量分数为30%,滤渣与热的浓硫酸反应产生的气体总质量为172g。 |
相似问题
东方中学课外活动小组在测定由氯化钠和硫酸钠形成混合物的组成时 进行了以下实验:取20g混合物全部溶于
东方中学课外活动小组在测定由氯化钠和硫酸钠形成混合物的组成时,进行了以下实验:取20g混合物全部溶于水,将得到的溶液等分为4份,然后分别加入一定量
我市盛产“福鼎黑”大理石 某中学化学兴趣小组通过实验测定这种大理石中碳酸钙的含量。将过量的稀盐酸加入
我市盛产“福鼎黑”大理石,某中学化学兴趣小组通过实验测定这种大理石中碳酸钙的含量。将过量的稀盐酸加入到20g大理石中(CaCO3+2HCl==CaCl2+H2O+CO2↑大
已知石灰石所含的杂质不溶于水和盐酸.为测定石灰石的纯度 取4 g样品于烧杯 将50 g稀盐酸分为5次
已知石灰石所含的杂质不溶于水和盐酸.为测定石灰石的纯度,取4 g样品于烧杯,将50 g稀盐酸分为5次依次加入烧杯,每次充分反应后,过滤、干燥、称量剩
为测定某未知浓度的氢氧化钡溶液的溶质质量分数 取某稀硫酸溶液20g 逐滴加入氢氧化钡溶液30g 同时
为测定某未知浓度的氢氧化钡溶液的溶质质量分数,取某稀硫酸溶液20g,逐滴加入氢氧化钡溶液30g,同时用pH计测定并记录反应过程中混合溶液pH变化情况(如
生产烧碱的工厂 常用便宜的原料纯碱和熟石灰制得成品。为模拟该生产过程 同学们取20gNa2CO3溶液
生产烧碱的工厂,常用便宜的原料纯碱和熟石灰制得成品。为模拟该生产过程,同学们取20gNa2CO3溶液与一定质量的饱和石灰水混合,恰好完全反应,得到4g白色












