在盛有10.0g氯化钠和碳酸氢钠固体混合物的锥形瓶中 加入143.4g稀盐酸 恰好完全反应 用仪器测
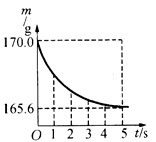
| 在盛有10.0g氯化钠和碳酸氢钠固体混合物的锥形瓶中,加入143.4g稀盐酸,恰好完全反应,用仪器测得锥形瓶连同药品的总质量(m)与反应时间(t)的关系如下图所示。 |
 |
| 试求: (1)原混合物中氯化钠的质量。 (2)稀盐酸中溶质HCl的质量。 (3)反应后所得溶液的溶质质量分数。 |
参考解答
| 解: (1)设原混合物中碳酸氢钠的质量为x,稀盐酸中溶质HCl的质量为y,生成的氯化钠质量为z。 产生CO2气体的质量:170.0g-165.6g=4.4g NaHCO3+HCl==NaCl+H2O+CO2↑ 84 36.5 58.5 44 x y z 4.4g 84/44=x/4.4g x=8.4g 原混合物中NaCl的质量为10.0g-8.4g=l.6g。 (2)36.5/44=y/4.4g y=3.65g (3)58.5/44=z/4.4g z=5.85g NaCl的总质量为1.6g+5.85g=7.45g。 反应后溶液的总质量为10.0g+143.4g-4.4g=149g。 反应后溶液中溶质的质量分数为(7.45g/149g)×100%=5%。 |
相似问题
汉墓出土青铜器表面一些有绿色物质 该物质俗称“铜绿” 其化学组成为Cu2(OH)2CO3。小明同学研
汉墓出土青铜器表面一些有绿色物质,该物质俗称“铜绿”,其化学组成为Cu2(OH)2CO3。小明同学研究该物质时做了下列实验。【实验一】 取2 22g “铜绿”
在科学实验中 常用电解水的方法制备纯净的氢气 供研究使用。试计算:电解1.8Kg水最多可制备的氢气质
在科学实验中,常用电解水的方法制备纯净的氢气,供研究使用。试计算:电解1 8Kg水最多可制备的氢气质量是多少? (电解水的反应化学方程式:2H2O2H2 ↑+O2 ↑)
某同学用13g锌与100g稀硫酸反应制取氢气 恰好完全反应 求生成氢气多少升?(提示:标准状态下氢气
某同学用13g锌与100g稀硫酸反应制取氢气,恰好完全反应,求生成氢气多少升?(提示:标准状态下氢气的密度为0 09g L;Zn + H2SO4 = ZnSO4 + H2↑)
电解水时 当电极上产生1.12升氧气时 有多少克水发生了电解?(氧气的密度约为1.43g/L 计算结
电解水时,当电极上产生1 12升氧气时,有多少克水发生了电解?(氧气的密度约为1 43g/L,计算结果保留一位小数)
为了培养自己解决实际化学问题的能力 李阳把家中厨房里的苏打和食盐各取若干混合 然后取该混合物进行实验
为了培养自己解决实际化学问题的能力,李阳把家中厨房里的苏打和食盐各取若干混合,然后取该混合物进行实验。如果他称取42 8g混合物加入到116g稀盐酸中恰












