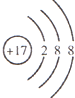
在海水的综合利用中 海水提溴工业是一个重要组成部分 其中一种提溴的工艺是在预先浓缩并酸化的海水中 通
在海水的综合利用中,海水提溴工业是一个重要组成部分,其中一种提溴的工艺是在预先浓缩并酸化的海水中,通入足量氯气,然后使生成的溴与吸收剂SO2反应转化为氢溴酸以达到富集溴元素的目的.有关上述工艺流程的以下化学用语中,不正确的是( )
|
参考解答
A.阴离子的电子式要用[把电子和元素符合括起来,溴离子最外层有8个电子,其电子式为: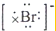 ,故A正确; B.氯气和溴离子能发生置换反应生成溴和氯离子,离子反应方程式为:2Br-+Cl2=Br2+2Cl-,故B正确; C.氯离子核外有3个电子层,最外层有8个电子,其离子结构示意图为: 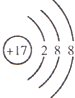 ,故C正确; D.溴具有强氧化性,二氧化硫具有还原性,二氧化硫和溴、水能发生氧化还原反应生成氢溴酸和硫酸,反应方程式为:2H2O+SO2+Br2=H2SO4+2HBr,故D错误; 故选D. |
相似问题
下列离子方程式正确的是( )A.FeCl3溶液与铜反应:Fe3++Cu═Fe2++Cu2+B.氢氧
下列离子方程式正确的是( )A.FeCl3溶液与铜反应:Fe3++Cu═Fe2++Cu2+B.氢氧化镁与醋酸反应:Mg(OH)2+2H+═Mg2++2H2OC.C12与NaOH溶液反应Cl2+2O
下列离子方程式书写正确的是( )A.向氯化铝溶液中加入过量氨水:A13++4NH3?H2O═A10
下列离子方程式书写正确的是( )A.向氯化铝溶液中加入过量氨水:A13++4NH3?H2O═A102-+4NH4++2H2OB.甲醛与足量银氨溶液共热:HCHO+2[Ag(NH3)2]++
(1)向用氯化铁溶液刻制印刷电路后的废液中 加入足量铁粉 发生反应的离子方程式是______ ___
(1)向用氯化铁溶液刻制印刷电路后的废液中,加入足量铁粉,发生反应的离子方程式是______、______.(2)实验室向某溶液中加入硫氰化钾溶液,无现象,
下列有关反应的离子方程式的书写中 不正确的是( )A.小苏打与氢氧化钠溶液混合:HCO3-+OH-
下列有关反应的离子方程式的书写中,不正确的是( )A.小苏打与氢氧化钠溶液混合:HCO3-+OH-═CO32-+H2OB.向溴化亚铁溶液中通入少量的Cl2:Cl2+2Br-
(1)写出下列物质在水中的电离方程式:①CuCl2______②NaHCO3______③KHSO4
(1)写出下列物质在水中的电离方程式:①CuCl2______②NaHCO3______③KHSO4______(2)按要求写出下列反应的离子方程式①氢氧化铜溶于盐酸______②硫酸