某学生利用以下装置探究纯净干燥的氯气与氨气之间的反应.回答下列问题:(1)根据下列所给试剂 选择制取
某学生利用以下装置探究纯净干燥的氯气与氨气之间的反应.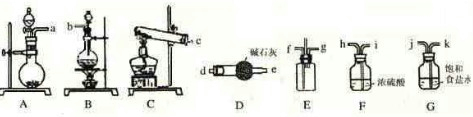 回答下列问题: (1)根据下列所给试剂,选择制取氨气的装置是(填对应字母)______;写出制备氯气的离子反应方程式______. 二氧化锰、碱石灰、浓盐酸、浓氨水、烧碱、生石灰 (2)已知,E装置是用于使纯净干燥的氯气与氨气发生反应的装置,试说明该装置的设计意图:______. (3)根据实验目的,所选装置的连接顺序为(填装置的接口字母):______接______,______接( f ),( g )接______,______接______,______接______;其中,G装置的作用是______. (4)氯气和氨气在常温下相混合就会发生反应生成氯化铵和氮气,该反应的化学方程式为:______;其中,氧化剂与还原剂的物质的量之比是______. (5)请你评价此套装置有何缺点______. |
参考解答
| (1)根据提供的药品,应用浓氨水和碱石灰或生石灰反应制备氨气,可用A装置,实验室用二氧化锰和浓盐酸反应制备氯气,反应的离子方程式 为MnO2+4H++2C1-
(2)由于氨气的密度小,氯气的密度大,密度小氨气的从长管进入向上扩散,密度大的氯气从短管进入向下扩散,这样能较快的充分的混合,具体操作为将比空气轻的氨气从长管口f进入,比空气重的氯气从短管口g进入,使反应气体逆流接触充分反应,中间导管用于排出空气以减少内部压力, 故答案为:将比空气轻的氨气从长管口f进入,比空气重的氯气从短管口g进入,使反应气体逆流接触充分反应,中间导管用于排出空气以减少内部压力; (3)装置A制取氨气,可用浓氨水与碱石灰(或烧碱或生石灰等),B装置中盛放的碱石灰,用来干燥氨气;G装置中盛放的饱和食盐水,用来除去氯气中混有的氯化氢气体;F装置用来干燥氯气,然后在E中混合反应,则连接顺序为a接d,e接f,g接h,i接j,k接b, 故答案为:a;d;e;h;i;j;k;b;除去C12中的HCl气体; (4)氯气和氨气在常温下相混合就会发生反应生成氯化铵和氮气,反应的化学方程式为3C12+8NH3=6NH4Cl+N2,由化合价的变化可以看出,当3mol氯气参加反应时,有2mol氨气被氧化,所以氧化剂和还原剂的物质的量之比为3:2, 故答案为:3C12+8NH3=6NH4Cl+N2;3:2; (5)氯气和氨气都污染空气,不能直接排放到空气中,实验缺少尾气处理装置, 故答案为:缺少尾气处理装置,造成空气污染. |
相似问题
如图所示 在干燥的圆底烧瓶中充满某气体a 胶头滴管中吸有少量液体b 当把溶液b挤进烧瓶后 打开止水夹
如图所示,在干燥的圆底烧瓶中充满某气体a,胶头滴管中吸有少量液体b,当把溶液b挤进烧瓶后,打开止水夹不能形成“喷泉”的组合是( )干燥气体a液体b
下列物质中 含有氯分子的是( )A.盐酸B.新制氯水C.液氯D.次氯酸
下列物质中,含有氯分子的是( )A.盐酸B.新制氯水C.液氯D.次氯酸
下列化合物中 不能由单质直接化合而得到的是( )A.NaClB.FeCl2C.FeCl3D.CuC
下列化合物中,不能由单质直接化合而得到的是( )A.NaClB.FeCl2C.FeCl3D.CuCl2
下列浓度关系正确的是( )A.氯水中:c(Cl2)=2[c(ClO-)+c(Cl-)+c(HClO
下列浓度关系正确的是( )A.氯水中:c(Cl2)=2[c(ClO-)+c(Cl-)+c(HClO)]B.新制氯水中:c(H+)>c(Cl-)>c(ClO-)C.等体积等浓度的氢氧
现有某纯净气体A 取标准状况下体积均为2.24L的两份样品 一份与过量的O2混合 燃烧后无固体物质生
现有某纯净气体A,取标准状况下体积均为2 24L的两份样品,一份与过量的O2混合,燃烧后无固体物质生成,气体生成物均被过量的澄清石灰水吸收,得到13 90g












