某同学设计了以下流程来检验碳酸钠粉末中可能含有少量氯化钠和氢氧化钠中的一种或两种杂质。(1)步骤1所
某同学设计了以下流程来检验碳酸钠粉末中可能含有少量氯化钠和氢氧化钠中的一种或两种杂质。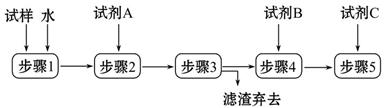 (1)步骤1所需玻璃仪器是______;步骤3的操作名称是______。 (2)对检验碳酸钠粉末中可能含有的杂质提出合理假设: 假设1:只含有氯化钠; 假设2:只含有___________; 假设3:氯化钠和氢氧化钠都含有。 (3)设计实验方案,进行实验。 限选以下试剂:氯化钡溶液、硝酸钡溶液、酚酞试液、稀硝酸、稀盐酸、稀硫酸、硝酸银溶液。回答下列问题: ①加入过量试剂A的名称是______。 ②填写下表:
|
参考解答
| (1)烧杯、玻璃棒 过滤 (2)氢氧化钠 (3)①硝酸钡溶液 ②
|
| (1)根据流程图可知,步骤1为溶解过程,所需玻璃仪器是烧杯和玻璃棒;步骤3为过滤操作。 (2)由题意可知,检验碳酸钠粉末中含有的杂质有三种可能: 可能1:只含有氯化钠;可能2:只含有氢氧化钠;可能3:氯化钠和氢氧化钠都含有。 (3)由于三种物质的区别在于阴离子,所以检验碳酸钠粉末中可能含有的杂质时,应该先除去CO32-,然后再检验溶液中是否含有OH-、Cl-,除去时不能引入OH-和Cl-。 ①加入过量试剂A的目的是除去CO32-,应该选用硝酸钡溶液,不能选用氯化钡溶液。 ②检验OH-时可以选用酚酞试液,检验Cl-时可以选用硝酸银溶液,但应该先检验OH-,因为用硝酸银溶液检验Cl-时OH-会造成干扰。可设计实验步骤如下:
|
相似问题
下列金属分别投入冷水中 能产生气体的是[ ]A.FeB.AlC.NaD.Zn
下列金属分别投入冷水中,能产生气体的是[ ]A.FeB.AlC.NaD.Zn
下列物质不能由相应的单质直接反应制取的是( )A.Na2O2B.FeCl3C.Na2OD.FeCl
下列物质不能由相应的单质直接反应制取的是( )A.Na2O2B.FeCl3C.Na2OD.FeCl2
某小组的同学对放置已久的过氧化钠的成分进行探究 请回答下列问题:(1)反应2Na2O2+2H2O==
某小组的同学对放置已久的过氧化钠的成分进行探究,请回答下列问题:(1)反应2Na2O2+2H2O===4NaOH+O2↑的还原剂是________(写化学式);反应2Na2O2+2CO2
下列关于钠的叙述中 不正确的是 [ ]A.钠燃烧时发出黄色的火焰 B.钠燃烧时生成氧化钠 C
下列关于钠的叙述中,不正确的是 [ ]A.钠燃烧时发出黄色的火焰 B.钠燃烧时生成氧化钠 C.实验室少量钠需保存在煤油中 D.钠原子的最外层只有一个电子
NA代表阿伏加德罗常数。常温常压下二氧化碳和过氧化钠反应后 若固体质量增加了28g 对该反应的分析
NA代表阿伏加德罗常数。常温常压下二氧化碳和过氧化钠反应后,若固体质量增加了28g,对该反应的分析,错误的是A.反应前后物质中阴、阳离子数目保持不变












