漂白粉是一种常用的消毒剂。(1)工业上生产漂白粉反应的化学方程式为:________________
| 漂白粉是一种常用的消毒剂。 (1)工业上生产漂白粉反应的化学方程式为:________________ __,漂白粉的有效成分为 。 (2)某探究小组从市场上购买了一袋包装破损的漂白粉,对该漂白粉的成分进行探究。根据下列试剂,设计实验方案,进行实验。请在答题卡上完成实验报告。 限选试剂:2mol·L-1NaOH溶液、2mol·L-1HCl溶液、2mol·L-1HNO3溶液、0.5mol·L-1BaCl2溶液、0.01mol·L-1AgNO3溶液、澄清石灰水、石蕊试液、酚酞试液、蒸馏水。
(3)探究小组为测定漂白粉中Ca(ClO)2的含量:称取漂白粉bg加水溶解后配制成100mL溶液,准确量取25.00mL于锥形瓶并加入足量盐酸和KI溶液,充分反应后,溶液中的游离碘用0.1000mol/L的Na2S2O3溶液滴定,滴定2次,平均消耗Na2S2O3溶液20.00mL。则该漂白粉中Ca(ClO)2的质量分数为_____________ _。(只列算式,不做运算,已知:Mr[Ca(ClO)2]="143" ;Ca(ClO)2+4HCl=2Cl2↑+CaCl2+2H2O,2Na2S2O3+I2=Na2S4O6+2NaI) |
参考解答
| (17分) (1)2Ca(OH)2+2Cl2=CaCl2+ Ca(ClO)2+2H2O (3分) Ca(ClO)2(1分) (2)
(说明:1、试剂用量不准确,整题合扣1分; 2、其他合理即给分) (3) 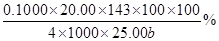 或 或 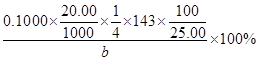 或 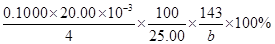 (3分,有效数字不准确,扣1分) (3分,有效数字不准确,扣1分) |
试题分析:(1)工业上用氯气和足量氢氧化钙反应制漂白粉,即2Ca(OH)2+2Cl2=CaCl2+ Ca(ClO)2+2H2O;漂白粉的有效成分是次氯酸钙,即Ca(ClO)2;(2)步骤2:若漂白粉变质,由于碳酸的酸性比次氯酸强,则次氯酸钙与空气中的CO2、H2O能发生复分解反应,即Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO,因此漂白粉溶于水后所得沉淀可能是碳酸钙;盐酸的酸性比碳酸强,若沉淀溶于足量2mol/LHCl溶液,产生的气体能使足量澄清石灰水变浑浊,或者产生的气体先使澄清石灰水变浑浊,后又变澄清,说明漂白粉已经部分变质或完全变质,其中含有CaCO3;步骤3:酚酞先遇碱性溶液变红,后遇次氯酸盐溶液褪色,根据结论推断,向A管中加入几滴或少量酚酞溶液,振荡,溶液先变红后褪色的,说明该漂白粉部分变质,含有Ca(ClO)2,可能含有Ca(OH)2;步骤4:向B管中先滴入足量2mol/LHNO3溶液、后滴入少量0.01mol/LAgNO3溶液,产生白色沉淀,说明该漂白粉中含有CaCl2;(3)由于n=c?V,则每次滴定平均消耗0.1000×20.00×10—3molNa2S2O3;由于2Na2S2O3+I2=Na2S4O6+2NaI中各物质的系数之比等于物质的量之比,则与Na2S2O3反应的I2为0.1000×20.00×10—3/2mol;由于 Cl2+2KI=2KCl+I2中各物质的系数之比等于物质的量之比,则置换出I2需要0.1000×20.00×10—3/2mol Cl2;由于Ca(ClO)2+4HCl=2Cl2↑+CaCl2+2H2O中各物质的系数之比等于物质的量之比,则25.00mL漂白粉溶液中含有的Ca(ClO)2为0.1000×20.00×10—3/4mol;100mL漂白粉溶液中含有的Ca(ClO)2为0.1000×20.00×10—3/4×100/25.00mol,由于m=n?M、Mr[Ca(ClO)2=143,则100mL漂白粉溶液中含有的0.1000×20.00×10—3/4×100/25.00×143gCa(ClO)2,则漂白粉中Ca(ClO)2的质量分数为0.1000×20.00×10—3/4×100/25.00×143/b×100%。 |
相似问题
某同学用下列装置验证一些物质的性质。下列说法正确的是A.Ⅰ图中:将胶头滴管中的水滴入到金属钠中 能看
某同学用下列装置验证一些物质的性质。下列说法正确的是A.Ⅰ图中:将胶头滴管中的水滴入到金属钠中,能看到U型管左侧红墨水上升B.Ⅱ图中:观察到湿润的
世界上60%的镁是从海水中提取的 其主要步骤如下:①把贝壳制成生石灰;②在海水中加入生石灰 过滤 洗
世界上60%的镁是从海水中提取的,其主要步骤如下:①把贝壳制成生石灰;②在海水中加入生石灰,过滤,洗涤沉淀物;③将沉淀物与盐酸反应,结晶、过滤;
工业上或实验室提纯以下物质的方法不合理的是(括号内为杂质)( )A.溴苯(溴):加NaOH溶液
工业上或实验室提纯以下物质的方法不合理的是(括号内为杂质)( )A.溴苯(溴):加NaOH溶液,分液B.MgCl2溶液(Fe3+):加MgO固体,过滤C.乙酸(水):
除去下列各组物质中的杂质选用的试剂和方法均最合理的是 物质杂质试剂方法A苯苯酚溴水过滤B二氧化碳二氧
除去下列各组物质中的杂质选用的试剂和方法均最合理的是物质杂质试剂方法A苯苯酚溴水过滤B二氧化碳二氧化硫澄清石灰水洗气C氧化铁二氧化硅氢氧化钠溶液过
不用其他试剂鉴别:①NaOH ②KCl ③Mg(NO3)2 ④CuSO4等四种溶液 先直接鉴别出一种
不用其他试剂鉴别:①NaOH、②KCl、③Mg(NO3)2、④CuSO4等四种溶液,先直接鉴别出一种,再逐一鉴别其余物质,则正确操作顺序是( )。A.④①②③B.①④












