某校探究学习小组同学用含有少量杂质(主要为少量泥沙 CaCl2 MgCl2 Na2SO4等)的粗盐制
某校探究学习小组同学用含有少量杂质(主要为少量泥沙、CaCl2、MgCl2、Na2SO4等)的粗盐制取“化学纯”级的NaCl,实验前他们设计了如下方案(框图)。 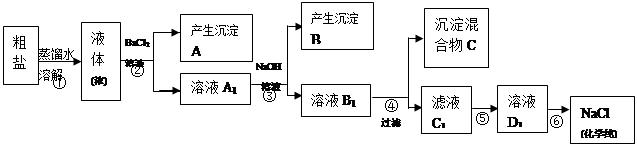 (1)请写出操作第④、⑤步所加试剂名称及第⑥步操作名称:④ ,⑤ ,⑥ ; (2) 沉淀混合物C的化学成分有(用文字和化学式表示): ; (3)写出第⑤步操作中可能发生反应的离子方程式: ; (4)如何用最简单方法检验第⑤步实验是否达到了目的: ; (5)你认为该设计里哪些步骤调换后不影响实验结果: ; (6)有同学认为上述实验设计步骤可以简化,请你提出简化的一种设想: 。 |
参考解答
⑴④碳酸钠溶液 ⑤盐酸 ⑥蒸发(蒸发结晶也可)(各1分) ⑵ 泥沙、BaSO4、BaCO3、CaCO3、Mg(OH)2(2分) ⑶第⑤步:H+ + OH- = H2O (1分) CO32- + 2H+ = H2O + CO2↑(1分) ⑷ 用玻璃棒蘸取溶液点在pH试纸中部,若变红,说明溶液呈酸性,无OH-、CO32-存在;若变蓝,说明溶液仍呈碱性,有OH-、CO32-存在,需继续滴加盐酸至呈酸性。(2分) ⑸②和③或③和④(2分) ⑹ 用Ba (OH)2代替BaCl2和NaOH,使②③步合并为一步(1分) |
试题分析:(1)分析流程图已给出的试剂的作用,BaCl2溶液除去Na2SO4,NaOH溶液除去MgCl2,所以④的作用为除去CaCl2,所选试剂为Na2CO3溶液,⑤的作用是除去过量的NaOH、Na2CO3,应选用盐酸,⑥的作用是从NaCl溶液中得到化学纯NaCl,为蒸发操作。 (2)BaCl2、NaOH、Na2CO3反应后得到的沉淀共有:泥沙、BaSO4、BaCO3、CaCO3、Mg(OH)2。 (3)第⑤步加入HCl,与NaOH和Na2CO3反应,所以离子方程式为:H+ + OH- = H2O; CO32- + 2H+ = H2O + CO2↑。 (4)HCl足量时第⑤步达到了目的,可用pH试纸检验,若试纸变化,证明HCl过量,OH ̄、CO32 ̄不存在,若变蓝,说明还有OH ̄、CO32 ̄,需继续滴加盐酸至呈酸性。 (5)NaOH不影响其他物质的除去,所以NaOH的加入顺序可以提前,也可以向后调整,即②和③或③和④可调换。 (6)用Ba (OH)2代替BaCl2和NaOH,可同时除去Na2SO4和MgCl2,使②③步合并为一步。 |
相似问题
草酸(乙二酸)可作还原剂和沉淀剂 用于金属除锈 织物漂白和稀土生产。一种制备草酸(含2个结晶水)的工
草酸(乙二酸)可作还原剂和沉淀剂,用于金属除锈、织物漂白和稀土生产。一种制备草酸(含2个结晶水)的工艺流程如右:回答下列问题:(1)CO和NaOH在一定条
高铁酸钾是一种新型高效多功能水处理剂。工业上常采用NaClO氧化法生产 反应原理为:①在碱性条件下
高铁酸钾是一种新型高效多功能水处理剂。工业上常采用NaClO氧化法生产,反应原理为:①在碱性条件下,利用NaClO氧化Fe(NO3)3制得Na2FeO43NaClO + 2Fe(N
某校化学小组的同学将一批废弃的线路板简单处理后 得到Cu Al Fe及少量Au Pt等金属的混合物
某校化学小组的同学将一批废弃的线路板简单处理后,得到Cu、Al、Fe及少量Au、Pt等金属的混合物,并设计了如下制备强酸铜和硫酸铝晶体的方案:回答下列问
有学生用五氧化二磷作为乙醇脱水制乙烯的催化剂 进行相关实验。按右表所示的量和反应条件在三颈瓶中加入一
有学生用五氧化二磷作为乙醇脱水制乙烯的催化剂,进行相关实验。按右表所示的量和反应条件在三颈瓶中加入一定量P2O5,并注入95%的乙醇,并加热,观察现象
有机物的除杂方法中正确的是(括号中的是杂质)A.乙酸(乙醛):加入新制的氢氧化铜 加热B.苯(苯酚)
有机物的除杂方法中正确的是(括号中的是杂质)A.乙酸(乙醛):加入新制的氢氧化铜,加热B.苯(苯酚):加入溴水,过滤C.溴乙烷(溴单质):加入热氢












