关于下列几种离子晶体 说法不正确的是( )A.由于NaCl 晶体和CsCl晶体中正负离子半径比不
关于下列几种离子晶体,说法不正确的是( )
|
参考解答
| D |
| A、正确,氯化钠配位数为6,氯化铯的配位数为8; B、是由于电荷不相同引起的,正确。 C、离子晶体,电荷越多,半径越小,晶格能越大; D、熔沸点与分解温度不是一回事。错误 |
相似问题
关于晶体的下列说法正确的是A.晶体中只要有阴离子就一定有阳离子B.晶体中只要有阳离子就一定有阴离子C
关于晶体的下列说法正确的是A.晶体中只要有阴离子就一定有阳离子B.晶体中只要有阳离子就一定有阴离子C.原子晶体的熔点一定比金属晶体的高D.分子晶体
(16分)观察下列部分图形 并按要求回答下列问题(1)由金刚石晶体结构和晶胞图知 金刚石是原子晶体
(16分)观察下列部分图形,并按要求回答下列问题(1)由金刚石晶体结构和晶胞图知,金刚石是原子晶体,晶体中碳原子取杂化轨道形成σ键,每个晶胞中含碳原
下列叙述正确的是( )A 固体时能导电的晶体一定为金属晶体B 电负性差值小于1.7的A B两种元素
下列叙述正确的是()A固体时能导电的晶体一定为金属晶体B电负性差值小于1 7的A、B两种元素,组成的化合物也可能为离子化合物C某晶体难溶于水、熔点高、
(13分)(1)下列物质在固态时 属于分子晶体的有 属于原子晶体的 属
(13分)(1)下列物质在固态时,属于分子晶体的有,属于原子晶体的,属于离子晶体的有。①金刚石②氩③水晶④水银⑤氧化铝⑥P4⑦苯(2)比较下列物质的有关
分析化学中常用X射线研究晶体结构 有一种蓝色晶体可表示为:[MxFey(CN)z] 研究表明它的结构
分析化学中常用X射线研究晶体结构,有一种蓝色晶体可表示为:[MxFey(CN)z],研究表明它的结构特性是Fe2+、Fe3+分别占据立方体的顶点,自身互不相邻,而CN


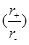 不相等,所以两晶体中离子的配位数不相等
不相等,所以两晶体中离子的配位数不相等









